Hvorfor foretrækkes dinatriumsalt af EDTA frem for EDTA?
Opløselighed: Dinatrium EDTA er mere opløseligt i vand end EDTA. Det skyldes, at natriumionerne i dinatriumsaltet er med til at bryde brintbindingerne mellem EDTA-molekylerne op, hvilket gør dem mere opløselige. Den højere opløselighed af dinatrium-EDTA muliggør fremstilling af opløsninger med højere koncentration, hvilket kan være fordelagtigt til visse anvendelser.
Stabilitet: Dinatrium EDTA er mere stabil i opløsning end EDTA. EDTA kan undergå hydrolyse i vandige opløsninger, hvilket fører til dannelse af metalkomplekser og frigivelse af protoner. Dette kan sænke opløsningens pH og reducere effektiviteten af EDTA som et chelateringsmiddel. Dinatriumsaltet af EDTA er mindre modtageligt for hydrolyse, hvilket betyder, at det kan bevare sine chelaterende egenskaber over et bredere område af pH-værdier.
pH: Dinatrium EDTA har en højere pH end EDTA. Det skyldes, at natriumionerne i dinatriumsaltet er med til at neutralisere de protoner, der frigives af EDTA-molekylerne. Den højere pH af dinatrium EDTA gør det mindre ætsende på metaloverflader og biologiske væv. Dette kan være en vigtig overvejelse i applikationer, hvor EDTA bruges som rengøringsmiddel eller i medicinske procedurer.
Samlet set gør den højere opløselighed, stabilitet og pH af dinatrium EDTA det til det foretrukne valg til mange anvendelser.
Sidste artikelHvad er ordligningen for saltsyrezink?
Næste artikelHvor mange elektroner omgiver det centrale atom i IF3?
 Varme artikler
Varme artikler
-
 Vandoverfladen er et fantastisk sted for kemiske reaktionerKredit:Pixabay/CC0 Public Domain Ved at bruge en avanceret teknik, forskere fra RIKEN-klyngen for banebrydende forskning har påvist, at en kemisk reaktion drevet af lys finder sted ti tusinde gang
Vandoverfladen er et fantastisk sted for kemiske reaktionerKredit:Pixabay/CC0 Public Domain Ved at bruge en avanceret teknik, forskere fra RIKEN-klyngen for banebrydende forskning har påvist, at en kemisk reaktion drevet af lys finder sted ti tusinde gang -
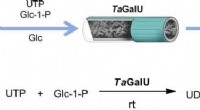 Trin for trin til slutproduktet gennem enzymkatalyseGrafisk abstrakt. Kredit:DOI:10.1016/j.cej.2021.131439 Enzymer (f.eks. dem, der stammer fra bakterier) kan omdanne en lang række forskellige udgangsmaterialer til et væld af målprodukter. Den såka
Trin for trin til slutproduktet gennem enzymkatalyseGrafisk abstrakt. Kredit:DOI:10.1016/j.cej.2021.131439 Enzymer (f.eks. dem, der stammer fra bakterier) kan omdanne en lang række forskellige udgangsmaterialer til et væld af målprodukter. Den såka -
 Kemikere udvikler en bioinspireret strategi til kontrolleret syntese af polyenerLysdrevet flip af alkengeometri. Kredit:Ryan Gilmour De forekommer i naturen, er reaktive og spiller en rolle i mange biologiske processer:polyener. Det er ikke underligt, at kemikere i lang tid h
Kemikere udvikler en bioinspireret strategi til kontrolleret syntese af polyenerLysdrevet flip af alkengeometri. Kredit:Ryan Gilmour De forekommer i naturen, er reaktive og spiller en rolle i mange biologiske processer:polyener. Det er ikke underligt, at kemikere i lang tid h -
 Foring af MOF-lommer til at detektere skadelige gasserSvovldioxidmolekyler (røde og gule) optages selektivt af porer i den metalorganiske struktur. Kredit:Valeriya Chernikova Et porøst materiale med skræddersyede lommer syet ind i dets struktur er et
Foring af MOF-lommer til at detektere skadelige gasserSvovldioxidmolekyler (røde og gule) optages selektivt af porer i den metalorganiske struktur. Kredit:Valeriya Chernikova Et porøst materiale med skræddersyede lommer syet ind i dets struktur er et
- Med alle fastklemt indendørs, esport er klar til tid i solen
- Video:Gør melatonin noget?
- Forklar kilden til signaler detekteret af elektromyogramelektroder?
- WeWork-stifter Adam Neumann fjernet fra Forbes milliardærliste
- Hvordan man tackler klimaændringer, fødevaresikkerhed og jordforringelse
- Hvad er ekspansionsforholdet for vandfri ammoniak?


