Hvordan tegner man en lithium- og aluminium-ionbinding?
1. Tegn Lewis-strukturerne for lithium og aluminium.
Lithium har en valenselektron, mens aluminium har tre. Lewis-strukturerne for disse elementer er:
Li:.Li
Al:.Al(.
2. Bestem ladningerne af de dannede ioner.
Lithium vil miste en elektron for at blive en positivt ladet lithiumion (Li+), mens aluminium vil få tre elektroner til at blive en negativt ladet aluminiumion (Al3-).
3. Tegn ionbindingen.
Ionbindingen er repræsenteret af en pil, der peger fra den positive ion (Li+) til den negative ion (Al3-). Den resulterende ionforbindelse er lithiumaluminiumhydrid (LiAlH4).
Strukturformlen for lithiumaluminiumhydrid er:
Li(+)---AlH4(-)
Denne formel viser overførslen af elektroner mellem lithium og aluminium, hvilket resulterer i dannelsen af en ionbinding mellem disse elementer.
 Varme artikler
Varme artikler
-
 Rammediversitet af carbonnitrider tilbyder rig platform for enkeltatoms katalyseOptimerede Pd-koordinationssteder inden for forskellige kulnitridstilladser med 6N, 9N, og 15N lommer. Værdier i parentes under hvert billede angiver de tilsvarende formationsenergier (venstre), bereg
Rammediversitet af carbonnitrider tilbyder rig platform for enkeltatoms katalyseOptimerede Pd-koordinationssteder inden for forskellige kulnitridstilladser med 6N, 9N, og 15N lommer. Værdier i parentes under hvert billede angiver de tilsvarende formationsenergier (venstre), bereg -
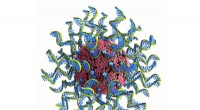 Ny maskinlæringsteknik analyserer hurtigt nanomedicin til kræftimmunterapiSNAer er kuglelignende former for DNA og RNA arrangeret på overfladen af en nanopartikel. Kredit:Chad Mirkin/Northwestern University Sfæriske nukleinsyrer er en klasse af personlig medicin til
Ny maskinlæringsteknik analyserer hurtigt nanomedicin til kræftimmunterapiSNAer er kuglelignende former for DNA og RNA arrangeret på overfladen af en nanopartikel. Kredit:Chad Mirkin/Northwestern University Sfæriske nukleinsyrer er en klasse af personlig medicin til -
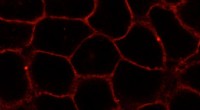 Hvordan forskere analyserer cellemembranerEn ny forbindelse, der efterligner naturligt kolesterol i membraner af levende celler (her:HeLa-celler). Stoffet er mærket med et fluorescerende farvestof (rødt). Kredit:L. Rakers et al./ Cell Chem B
Hvordan forskere analyserer cellemembranerEn ny forbindelse, der efterligner naturligt kolesterol i membraner af levende celler (her:HeLa-celler). Stoffet er mærket med et fluorescerende farvestof (rødt). Kredit:L. Rakers et al./ Cell Chem B -
 Forskning viser Krebs cyklus mulig uden metaller eller enzymkatalysatorer, giver nye ledetråde til …Trent Stubbs 20 i laboratorium med Furman kemiprofessor Greg Springsteen. Kredit:Jeremy Fleming, Furman Universitet Nylig Furman University-kandidat Trent Stubbs er forfatter til en ny undersøgels
Forskning viser Krebs cyklus mulig uden metaller eller enzymkatalysatorer, giver nye ledetråde til …Trent Stubbs 20 i laboratorium med Furman kemiprofessor Greg Springsteen. Kredit:Jeremy Fleming, Furman Universitet Nylig Furman University-kandidat Trent Stubbs er forfatter til en ny undersøgels
- Den menneskelige kreativitets psykologi hjælper kunstig intelligens med at forestille sig det ukend…
- Forskere gennemsøger skibsvrag fra Første Verdenskrig for at løse militært mysterium
- Struktureret lys og nanomaterialer åbner nye måder at skræddersy lys på nanoskala
- En magneto-optisk modulator kunne lette udviklingen af næste generation af superlederbaserede com…
- Hvad kigger du på?
- Facebook fritager politisk tale fra faktatjek


