Vil en forøgelse af mængden af begrænsende reaktant i en reaktion så øge det procentvise udbytte?
Den begrænsende reaktant er den reaktant, der helt forbruges i en kemisk reaktion, og derved begrænser mængden af produkt, der kan dannes. Forøgelse af mængden af den begrænsende reaktant vil ikke resultere i et højere procentudbytte, fordi der stadig vil være en utilstrækkelig mængde af den eller de andre reaktanter til at reagere med overskuddet af den begrænsende reaktant. Det procentvise udbytte bestemmes af mængden af produkt opnået i forhold til den teoretiske maksimale mængde produkt, der kunne dannes baseret på den afbalancerede kemiske ligning. For at øge det procentvise udbytte skal de relative mængder af reaktanterne justeres, så alle reaktanter er til stede i støkiometrisk korrekte proportioner, eller reaktionsbetingelserne skal optimeres.
 Varme artikler
Varme artikler
-
 Polymer til at fange ammoniakforurening realiseretAt arbejde i laboratoriet kan være lidt rodet. Dette skud er fra den faktiske produktion af polymeren på kemilaboratoriet. Men ligesom Heloisa Bordallos studerende siger:Ren lab =ingen arbejder! Kredi
Polymer til at fange ammoniakforurening realiseretAt arbejde i laboratoriet kan være lidt rodet. Dette skud er fra den faktiske produktion af polymeren på kemilaboratoriet. Men ligesom Heloisa Bordallos studerende siger:Ren lab =ingen arbejder! Kredi -
 Ny strategi forbedrer stabiliteten af platingruppemetalkatalysatorerKredit:ACS For nylig, en gruppe ledet af Prof. kalcinering, og udviklede en ny strategi for at forbedre stabiliteten af platinagruppemetaller (PGMer) katalysatorer. Denne undersøgelse blev offe
Ny strategi forbedrer stabiliteten af platingruppemetalkatalysatorerKredit:ACS For nylig, en gruppe ledet af Prof. kalcinering, og udviklede en ny strategi for at forbedre stabiliteten af platinagruppemetaller (PGMer) katalysatorer. Denne undersøgelse blev offe -
 Fremtidens MOF'er:Konvertering af krystallinske metal-organiske rammer til glas eller væskeKrystallinske MOFer bliver nu omdannet til glas/flydende tilstande, åbne nye applikationer. Kredit:Mindy Takamiya Metal-organiske rammer (MOFer) er porøse, krystallinske materialer, der kan fange
Fremtidens MOF'er:Konvertering af krystallinske metal-organiske rammer til glas eller væskeKrystallinske MOFer bliver nu omdannet til glas/flydende tilstande, åbne nye applikationer. Kredit:Mindy Takamiya Metal-organiske rammer (MOFer) er porøse, krystallinske materialer, der kan fange -
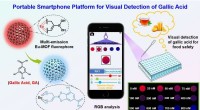 Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute
Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute


