Hvorfor kan farven på phenolphtalein langsomt forsvinde, selv efter at al syre er titreret?
1. Carbondioxidabsorption: Phenolphtalein er følsomt over for kuldioxid fra luften. Hvis opløsningen udsættes for luft under titreringen, kan kuldioxid opløses i vandet og reagere med det og danne kulsyre. Dette kan få opløsningens pH til at falde, hvilket resulterer i, at den lyserøde farve forsvinder.
2. Reaktion med stærke syrer: I nærvær af stærke syrer kan phenolphtalein undergå kemiske reaktioner, der fører til ødelæggelse af dets farve. Stærke syrer som saltsyre (HCl) eller svovlsyre (H2SO4) kan protonere phenolphtalein-molekylet, hvilket får det til at miste sin farve.
3. Fotonedbrydning: Langvarig eksponering for lys, især ultraviolet (UV) lys, kan forårsage nedbrydning af phenolphtalein. Dette kan resultere i, at den lyserøde farve falmer eller forsvinder over tid.
4. Temperatur: Høje temperaturer kan også påvirke stabiliteten af phenolphtalein. Hvis opløsningen opvarmes under titrering, kan farven begynde at falme på grund af den accelererede nedbrydning af indikatoren.
5. Urenheder: Tilstedeværelsen af urenheder i phenolphtaleinopløsningen eller den titrerede opløsning kan interferere med farveændringen. Visse urenheder kan reagere med indikatoren, hvilket får dens farve til at forsvinde eller ændre sig.
For at minimere disse effekter anbefales det at udføre titreringer hurtigt og præcist, minimere eksponering for luft og lys og bruge friske indikatorløsninger af høj kvalitet. Derudover kan det at holde opløsningen ved en moderat temperatur og undgå stærke syrer hjælpe med at bevare farven på phenolphtalein under titreringer.
Sidste artikelHvad har 7 valenselektroner i det periodiske system?
Næste artikelHvad er ordligningen for blycarbonat og svovlsyre?
 Varme artikler
Varme artikler
-
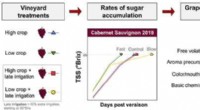 At bremse modningen af druer kan forbedre bærkvaliteten til vinfremstillingKredit:American Chemical Society Vindruer er særligt kræsne, når det kommer til deres miljø. For eksempel, hedebølger og tørke fører til tidligere bærmodning og glansløs vin. Og disse typer episod
At bremse modningen af druer kan forbedre bærkvaliteten til vinfremstillingKredit:American Chemical Society Vindruer er særligt kræsne, når det kommer til deres miljø. For eksempel, hedebølger og tørke fører til tidligere bærmodning og glansløs vin. Og disse typer episod -
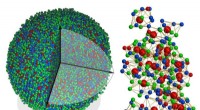 Århundrede gammelt problem løst med første gang nogensinde 3D-atomafbildning af et amorft fast st…Til venstre, en eksperimentel 3D -atommodel af en metallisk glas -nanopartikel, 8 nanometer i diameter. Ret, 3D -atomemballage af et superklynge i strukturen, med forskelligt farvede kugler, der repræ
Århundrede gammelt problem løst med første gang nogensinde 3D-atomafbildning af et amorft fast st…Til venstre, en eksperimentel 3D -atommodel af en metallisk glas -nanopartikel, 8 nanometer i diameter. Ret, 3D -atomemballage af et superklynge i strukturen, med forskelligt farvede kugler, der repræ -
 Iagttager ændringer i molekylernes chiralitet i realtidKirale molekyler - forbindelser, der er spejlbilleder af hinanden - spiller en vigtig rolle i biologiske processer og i kemisk syntese. Kemikere ved ETH Zürich er nu lykkedes for første gang at bruge
Iagttager ændringer i molekylernes chiralitet i realtidKirale molekyler - forbindelser, der er spejlbilleder af hinanden - spiller en vigtig rolle i biologiske processer og i kemisk syntese. Kemikere ved ETH Zürich er nu lykkedes for første gang at bruge -
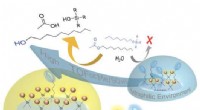 Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
- Modtagelse af en login -kode via SMS og e -mail er ikke sikker. Her er hvad du skal bruge i stedet
- Bioniske svampe smelter sammen nanoteknologi, bakterier og svampe
- Skal vi være nervøse over togrejser?
- Påvisning af hydrotermiske ventilationsåbninger i vulkanske søer
- Historien om antarktiske indlandsis har spor for vores fremtid
- Forskning løfter låget på pornografiens indflydelse


