Hvad er en kovalent forbindelse, der opløses i vand?
Vand er et meget polært molekyle med en delvis positiv ladning på brintatomerne og en delvis negativ ladning på iltatomet. Den delvise positive ende af den polære kovalente forbindelse tiltrækkes af den delvise negative ende af vandmolekylet og omvendt. Denne interaktion fører til opløsning af den kovalente forbindelse i vand og dannelse af en homogen opløsning.
Eksempler på kovalente forbindelser, der opløses i vand, omfatter:
1. Sukker (saccharose): Saccharose er en polær kovalent forbindelse, der almindeligvis anvendes som sødemiddel i forskellige fødevareprodukter. Forskellen i elektronegativitet mellem oxygen- og kulstofatomer skaber et dipolmoment, som gør det muligt for saccharose at interagere med vandmolekyler og danne en opløsning.
2. Ethylalkohol (ethanol): Ethanol er en polær kovalent forbindelse, der i vid udstrækning anvendes som opløsningsmiddel, desinfektionsmiddel og alkoholisk drik. Det elektronegative oxygenatom trækker elektroner væk fra brint- og kulstofatomerne, hvilket skaber partielle ladninger. Disse delvise ladninger tillader ethanol at opløses i vand.
3. Natriumchlorid (bordsalt): Selvom det primært består af ionbindinger, udviser natriumchlorid en grad af kovalent karakter på grund af den lille forskel i elektronegativitet mellem natrium og klor. Denne kovalente natur gør det muligt for natriumchlorid at have en vis opløselighed i vand, hvilket resulterer i den velkendte smag af salt i vandige opløsninger.
4. Acetone: Acetone er en polær kovalent forbindelse, der almindeligvis bruges som opløsningsmiddel til neglelakfjerner, malingfortynder og rengøringsmiddel. Carbonylgruppen (C=O) giver acetone dens polære karakter, så den kan interagere med vandmolekyler og opløses i vand.
Polaritet er en afgørende afgørende faktor for opløseligheden af kovalente forbindelser i vand. Mens ioniske og kovalente forbindelser er fundamentalt forskellige i deres kemiske binding, kan visse kovalente forbindelser med betydelige partielle ladninger etablere gunstige interaktioner med vand, hvilket gør dem i stand til at opløses og danne homogene blandinger.
 Varme artikler
Varme artikler
-
 Syntetisering af værdifulde kemikalier fra forurenet jordKredit:Unsplash/CC0 Public Domain Forskere ved Johannes Gutenberg University Mainz (JGU) og ETH Zürich har udviklet en proces til at producere råvarekemikalier på en meget mindre farlig måde, end
Syntetisering af værdifulde kemikalier fra forurenet jordKredit:Unsplash/CC0 Public Domain Forskere ved Johannes Gutenberg University Mainz (JGU) og ETH Zürich har udviklet en proces til at producere råvarekemikalier på en meget mindre farlig måde, end -
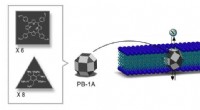 Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to
Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to -
 Enhed forvandler skaller af havdyr til kraft til medicinsk, augmented reality, mobiltelefonenhederEt Purdue-team er ved at omdanne rejeskalmateriale til en funktionel enhed til at generere elektricitet. Kredit:Purdue University En innovation, der bruger materiale, der stammer fra skaller fra k
Enhed forvandler skaller af havdyr til kraft til medicinsk, augmented reality, mobiltelefonenhederEt Purdue-team er ved at omdanne rejeskalmateriale til en funktionel enhed til at generere elektricitet. Kredit:Purdue University En innovation, der bruger materiale, der stammer fra skaller fra k -
 Cement, salt og vand:Et nyt lagermateriale til grøn varmeKredit:CC0 Public Domain Opvarmning af det rum, hvor vi bor eller arbejder, er en almindelig nødvendighed i de fleste beboede områder. Den energi, der kræves til denne proces, er ansvarlig for en
Cement, salt og vand:Et nyt lagermateriale til grøn varmeKredit:CC0 Public Domain Opvarmning af det rum, hvor vi bor eller arbejder, er en almindelig nødvendighed i de fleste beboede områder. Den energi, der kræves til denne proces, er ansvarlig for en


