Hvilken ville danne en elektrolytopløsning?
Nogle eksempler på stoffer, der danner elektrolytopløsninger omfatter:
- Syrer, såsom saltsyre (HCl) og svovlsyre (H2SO4)
- Baser, såsom natriumhydroxid (NaOH) og kaliumhydroxid (KOH)
- Salte, såsom natriumchlorid (NaCl) og kaliumnitrat (KNO3)
Når disse stoffer opløses i vand, opløses de i deres bestanddele. For eksempel, når natriumchlorid opløses i vand, opløses det i natriumioner (Na+) og chloridioner (Cl-). Disse ioner kan derefter frit bevæge sig rundt i opløsningen og bærer en elektrisk ladning med sig.
Elektrolytopløsninger er vigtige, fordi de spiller en rolle i mange biologiske processer, såsom nervetransmission, muskelsammentrækning og hjertefunktion. De bruges også i en række industrielle applikationer, såsom batterier, galvanisering og vandbehandling.
Sidste artikelHvad er en elektrolyt, når den placeres i vandig opløsning?
Næste artikelHvordan kredsede atomer gennem fødekæden?
 Varme artikler
Varme artikler
-
 Forskere opdager superelastisk formhukommelsesmaterialeMaterialevidenskab og ingeniørprofessor Seok-Woo Lee og kolleger har opdaget superelastiske formhukommelsesegenskaber i et materiale, der kunne bruges under de hårdeste forhold, såsom det ydre rum. Kr
Forskere opdager superelastisk formhukommelsesmaterialeMaterialevidenskab og ingeniørprofessor Seok-Woo Lee og kolleger har opdaget superelastiske formhukommelsesegenskaber i et materiale, der kunne bruges under de hårdeste forhold, såsom det ydre rum. Kr -
 Ny, ikke-invasive blodsukkermålingsmetoder ved hjælp af spytKredit:University of Waterloo På trods af banebrydende diabetesforskning gennem det sidste århundrede, mennesker med diabetes er stadig nødt til at stole på at få blodprøver for at overvåge deres
Ny, ikke-invasive blodsukkermålingsmetoder ved hjælp af spytKredit:University of Waterloo På trods af banebrydende diabetesforskning gennem det sidste århundrede, mennesker med diabetes er stadig nødt til at stole på at få blodprøver for at overvåge deres -
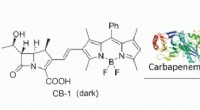 En fluorogen probe kan detektere aktiviteten af multidrug-resistente patogener i et assaysystemKredit:Wiley Carbapenemer er blandt sidste udvejs antibiotika og kan bekæmpe infektioner, hvor andre lægemidler længe har mistet deres effektivitet. Imidlertid, selv carbapenem-resistente patogene
En fluorogen probe kan detektere aktiviteten af multidrug-resistente patogener i et assaysystemKredit:Wiley Carbapenemer er blandt sidste udvejs antibiotika og kan bekæmpe infektioner, hvor andre lægemidler længe har mistet deres effektivitet. Imidlertid, selv carbapenem-resistente patogene -
 Superkritisk svar på spildolie fundetKredit:Pixabay/CC0 Public Domain Smøreolier nedbrydes og oxiderer ved brug samt akkumulerer partikler fra de motorer og andre maskiner, hvori de bruges. Ultimativt, deres effektivitet forværres, o
Superkritisk svar på spildolie fundetKredit:Pixabay/CC0 Public Domain Smøreolier nedbrydes og oxiderer ved brug samt akkumulerer partikler fra de motorer og andre maskiner, hvori de bruges. Ultimativt, deres effektivitet forværres, o
- Hvordan overfører familien kultur?
- Ubæredygtige fødevaresystemer:Kan vi vende nuværende tendenser?
- AI møder partikelteknologi for at forenkle flydeevne og pakkedensitetsforudsigelser
- En måneformørkelse kommer søndag:Vil Colorado være i stand til at se den?
- Sådan fungerer magneter
- Kælvningen af et massivt isbjerg fra Larsen C ishylde


