Hvor mange valenselektroner er repræsenteret i Lewis elektron-prikstrukturen for SO2?
For at bestemme antallet af valenselektroner i SO2 tilføjer vi valenselektronerne for hvert atom:
- Svovl (S):6 valenselektroner
- Ilt (O) x 2:2 x 6 =12 valenselektroner
I alt har SO2 6 + 12 =18 valenselektroner.
Lewis-strukturen viser dog 24 valenselektroner, fordi hver dobbeltbinding mellem svovl og oxygen bidrager med yderligere to elektroner til strukturen, og der er to dobbeltbindinger. Så 18 + 6 =24 valenselektroner.
 Varme artikler
Varme artikler
-
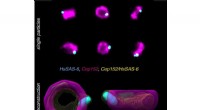 Superopløsningsmikroskopi bygger flerfarvet 3-D fra 2-DHumane centrioler mærket med antistoffer mod to proteiner (Cep152, HsSAS-6) og afbildet ved hjælp af superopløsningsmikroskopi. Fra mange individuelle partikler, der viser projektioner af centriolkomp
Superopløsningsmikroskopi bygger flerfarvet 3-D fra 2-DHumane centrioler mærket med antistoffer mod to proteiner (Cep152, HsSAS-6) og afbildet ved hjælp af superopløsningsmikroskopi. Fra mange individuelle partikler, der viser projektioner af centriolkomp -
 Ny teknik til at forbedre duktiliteten af keramiske materialer til missiler, motorerPurdue University-forskere har udviklet en ny proces for at hjælpe med at overvinde keramiks skøre natur og gøre den mere holdbar. Kredit:Purdue University/Chris Adam Noget så simpelt som et elekt
Ny teknik til at forbedre duktiliteten af keramiske materialer til missiler, motorerPurdue University-forskere har udviklet en ny proces for at hjælpe med at overvinde keramiks skøre natur og gøre den mere holdbar. Kredit:Purdue University/Chris Adam Noget så simpelt som et elekt -
 Brug nær-infrarødt lys til 3D-print et øre inde i kroppenIkke -invasiv in vivo 3D bioprinting auricle in situ. Kredit:Professor Maling Gou, State Key Laboratory of Biotherapy and Cancer Center, West China Hospital, Sichuan universitet. Et team af forske
Brug nær-infrarødt lys til 3D-print et øre inde i kroppenIkke -invasiv in vivo 3D bioprinting auricle in situ. Kredit:Professor Maling Gou, State Key Laboratory of Biotherapy and Cancer Center, West China Hospital, Sichuan universitet. Et team af forske -
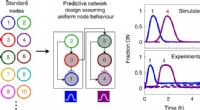 Et skridt mod skabelsen af materialer styret af kunstige generKredit:Samuel W. Schaffter et al., Nature Chemistry (2022). DOI:10.1038/s41557-022-01001-3 Vores kroppes gener arbejder sammen om at regulere, hvordan vores celler opfører sig. Hvis du f.eks. flår
Et skridt mod skabelsen af materialer styret af kunstige generKredit:Samuel W. Schaffter et al., Nature Chemistry (2022). DOI:10.1038/s41557-022-01001-3 Vores kroppes gener arbejder sammen om at regulere, hvordan vores celler opfører sig. Hvis du f.eks. flår
- Det er muligt at øge mængden af tryk med blankt område, hvor der påføres kraft?
- Rigid beslutningstagning kan skade samvittighedsfulde medarbejdere
- Vi skal slippe af med kulstof i atmosfæren, ikke kun reducere emissioner
- Bekæmpelse af bakteriel biofilmdannelse med titanium belagt med guld nanopartikler
- Findes eddikesyre i appelsinjuice?
- Nano for sanserne


