Hvordan er vand en væske?
Denne hydrogenbinding skaber en stærk tiltrækning mellem vandmolekyler, som holder dem sammen og forhindrer dem i at bevæge sig frit forbi hinanden. Som følge heraf har vand et relativt højt kogepunkt og et lavt frysepunkt sammenlignet med andre stoffer med lignende molekylvægt. Ved stuetemperatur er disse hydrogenbindinger stadig stærke nok til at holde vandmolekylerne sammen i flydende tilstand.
Vandets unikke egenskaber, herunder dets overfladespænding, kohæsion og høje specifikke varmekapacitet, er også påvirket af hydrogenbinding. Disse egenskaber er essentielle for mange organismers overlevelse og spiller en afgørende rolle i forskellige biologiske processer.
Sidste artikelHvad er forskellen mellem blanding og bestanddel?
Næste artikelHvad sker der med saltopløsningen efter fordampning?
 Varme artikler
Varme artikler
-
 Udvikling af ny fotovoltaisk kommercialiseringsteknologiProfessor Jongmin Choi, Institut for Energividenskab og Teknik, DGIST. Kredit:DGIST En teknologi til yderligere at fremskynde kommercialiseringen af Colloidal Quantum Dot (CQD) fotovoltaiske (PV
Udvikling af ny fotovoltaisk kommercialiseringsteknologiProfessor Jongmin Choi, Institut for Energividenskab og Teknik, DGIST. Kredit:DGIST En teknologi til yderligere at fremskynde kommercialiseringen af Colloidal Quantum Dot (CQD) fotovoltaiske (PV -
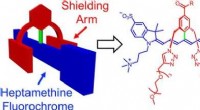 Stabile og funktionelle farvestoffer til nær-infrarød fluorescensbilleddannelse af levende individ…Kredit:Wiley Forskere kan overvåge biomolekylære processer i levende væv ved hjælp af ikke-invasive optiske metoder, såsom fluorescensbilleddannelse. Imidlertid, de fluorescerende farvestoffer, de
Stabile og funktionelle farvestoffer til nær-infrarød fluorescensbilleddannelse af levende individ…Kredit:Wiley Forskere kan overvåge biomolekylære processer i levende væv ved hjælp af ikke-invasive optiske metoder, såsom fluorescensbilleddannelse. Imidlertid, de fluorescerende farvestoffer, de -
 Materialer i lithium-ion-batterier kan genbruges til genbrugEt team af forskere, anført af Zhen (Jason) Han, professor i energi, miljø- og kemiteknik, udvikler en metode til genbrug af batteriers materialer. Kredit:Shutterstock Kina forventer at generere 2
Materialer i lithium-ion-batterier kan genbruges til genbrugEt team af forskere, anført af Zhen (Jason) Han, professor i energi, miljø- og kemiteknik, udvikler en metode til genbrug af batteriers materialer. Kredit:Shutterstock Kina forventer at generere 2 -
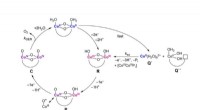 Selvhelbredende katalysatorer gør det lettere at lagre solenergi med vandSelvsamlingsvejen, der bruges til selvhelbredende katalysatorer. Kredit:Costentin et al. ©2017 PNAS (Phys.org) – I øjeblikket er en af de mest effektive måder at lagre solenergi på at overføre e
Selvhelbredende katalysatorer gør det lettere at lagre solenergi med vandSelvsamlingsvejen, der bruges til selvhelbredende katalysatorer. Kredit:Costentin et al. ©2017 PNAS (Phys.org) – I øjeblikket er en af de mest effektive måder at lagre solenergi på at overføre e
- Hvad former sammensætningen af mikrober i en sangfugls tarm?
- College ture for kinesiske teenagere et hurtigt voksende marked for turistindustrien
- Sikker, lavpris, modulopbygget, selvprogrammerende robotter
- Hvorfor eksploderer frosne kalkuner, når de frituresteges?
- Studerende demonstrerer gyldigheden af modeller, der bruger gratis, offentligt tilgængelige klima…
- Forskere diskuterer den fremtidige virkning af nutidens nanoteknologiske forskning


