Hvad afhænger atomers kemiske egenskaber af?
Følgende faktorer påvirker atomernes kemiske egenskaber:
1. Atomnummer: Et atoms atomnummer bestemmer antallet af protoner i dets kerne. Antallet af protoner i et atom bestemmer også antallet af elektroner, som atomet har.
2. Elektronkonfiguration: Et atoms elektronkonfiguration refererer til arrangementet af dets elektroner i orbitaler omkring kernen. Et atoms elektronkonfiguration bestemmer atomets kemiske egenskaber.
3. Ioniseringsenergi: Et atoms ioniseringsenergi er den energi, der kræves for at fjerne en elektron fra atomet. Et atoms ioniseringsenergi stiger, når antallet af protoner i kernen stiger. Det betyder, at atomer med højere ioniseringsenergier er mindre tilbøjelige til at miste elektroner og danne positive ioner.
4. Elektronaffinitet: Et atoms elektronaffinitet er den energiændring, der opstår, når et atom får en elektron. Et atoms elektronaffinitet stiger, når antallet af protoner i kernen stiger. Dette betyder, at atomer med højere elektronaffiniteter er mere tilbøjelige til at få elektroner og danne negative ioner.
5. Elektronegativitet: Et atoms elektronegativitet er et mål for dets evne til at tiltrække elektroner. Elektronegativiteten stiger, når antallet af protoner i kernen øges, og når antallet af valenselektroner falder.
Disse faktorer bestemmer, hvordan atomer interagerer med hinanden for at danne kemiske bindinger og forbindelser. Ved at forstå disse egenskaber kan kemikere forudsige, hvordan atomer vil opføre sig i forskellige kemiske reaktioner.
 Varme artikler
Varme artikler
-
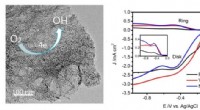 Ny elektrokatalysator udviklet til iltreduktionsreaktionVanadiumnitrid kvanteprikker forankret homogent på nitrogen-doteret grafen (VNQD-NG) blev fremstillet. De unikke strukturelle træk ved VNQD-NG inklusive de rigelige VN-kvantepunkter, højt overfladeare
Ny elektrokatalysator udviklet til iltreduktionsreaktionVanadiumnitrid kvanteprikker forankret homogent på nitrogen-doteret grafen (VNQD-NG) blev fremstillet. De unikke strukturelle træk ved VNQD-NG inklusive de rigelige VN-kvantepunkter, højt overfladeare -
 Bakteriefilm adskiller vand fra olieBakteriel cellulose viste nytte til at adskille olie og vand i eksperimenter ledet ved NC State. Kredit:Zahra Ashrafi Forskere har påvist, at en slimet, dog hård, type biofilm, som visse bakterier
Bakteriefilm adskiller vand fra olieBakteriel cellulose viste nytte til at adskille olie og vand i eksperimenter ledet ved NC State. Kredit:Zahra Ashrafi Forskere har påvist, at en slimet, dog hård, type biofilm, som visse bakterier -
 Nylige fremskridt inden for optimering af dispergerede platinkatalysatorerIndfødt platinklump, lokalitet Kondyor mine, Khabarovsk Krai, Rusland. Kredit:Wikipedia. Meget spredte platinkatalysatorer giver nye muligheder for industrielle processer, såsom den flammeløse for
Nylige fremskridt inden for optimering af dispergerede platinkatalysatorerIndfødt platinklump, lokalitet Kondyor mine, Khabarovsk Krai, Rusland. Kredit:Wikipedia. Meget spredte platinkatalysatorer giver nye muligheder for industrielle processer, såsom den flammeløse for -
 Kulfibre fra grønne prækursorer og optimerede processerKredit:fabiodevilla, Shutterstock Smarte materialer svarer på sammensatte komponenter for at tilbyde række af ønskede egenskaber, alligevel har de nuværende fremstillingsprocesser på nogle måder i
Kulfibre fra grønne prækursorer og optimerede processerKredit:fabiodevilla, Shutterstock Smarte materialer svarer på sammensatte komponenter for at tilbyde række af ønskede egenskaber, alligevel har de nuværende fremstillingsprocesser på nogle måder i
- Højteknologisk hjælp forbinder fans til off-the-grid Iditarod-løb
- Tidlige afrikanske muslimer havde kosmopolitiske, halal diæt, viser opdagelse af tusindvis af gamle…
- Metalholdige forbindelser viser lovende som HIV-våben
- Spring Constant (Hookes Law): Hvad er det og hvordan man beregner (w /enheder og formler)
- Undersøgelse af celledræbere:Et avanceret system til størrelsesafhængig cytotoksicitetsanalyse a…
- Sådan beregnes højde ud fra bind


