Hvordan beregner man massen af eddikesyre og bagepulver?
For at bestemme massen af eddikesyre (CH3COOH), du skal bruge til en kemisk reaktion, skal du kende følgende oplysninger:
1. Den afbalancerede kemiske ligning for reaktionen.
2. Den molære masse af eddikesyre.
3. Den ønskede mængde produkt eller reaktant.
Her er trinene til, hvordan man beregner massen af eddikesyre:
1. Bestem moleforholdet:
Fra den afbalancerede kemiske ligning skal du identificere molforholdet mellem eddikesyre og det ønskede produkt eller reaktant. For eksempel, hvis den balancerede ligning er:
```
CH3COOH + NaHCO3 → CO2 + H2O + CH3COONa
```
Molforholdet mellem eddikesyre (CH3COOH) og natriumbicarbonat (NaHCO3) er 1:1.
2. Beregn molmassen:
Bestem den molære masse af eddikesyre (CH3COOH). Den molære masse er summen af atommasserne af alle atomer i forbindelsen. For eddikesyre har vi:
Molær masse af CH3COOH =(2 × 12,01 g/mol) + (4 × 1,01 g/mol) + (2 × 16,00 g/mol) + (1 × 12,01 g/mol) =60,05 g/mol
3. Beregn de nødvendige modermærker:
Ud fra molforholdet og den ønskede mængde produkt eller reaktant skal du beregne antallet af mol eddikesyre, du har brug for. Lad os sige, at du vil producere 0,1 mol kuldioxid (CO2) fra reaktionen. Da molforholdet er 1:1, skal du også bruge 0,1 mol eddikesyre.
4. Konverter mol til masse:
Multiplicer antallet af mol eddikesyre (0,1 mol) med dens molære masse (60,05 g/mol) for at opnå den nødvendige masse af eddikesyre:
Masse af CH3COOH =0,1 mol × 60,05 g/mol =6,005 g
Derfor skal du bruge cirka 6,01 gram eddikesyre for at producere 0,1 mol kuldioxid i den givne reaktion.
Beregning af massen af bagepulver til en kemisk reaktion
Processen med at beregne massen af bagepulver (natriumbicarbonat, NaHCO3) for en kemisk reaktion følger lignende principper:
1. Balanceret kemisk ligning:
Start med den afbalancerede kemiske ligning for reaktionen, der involverer bagepulver.
2. Molar masse bagepulver:
Bestem den molære masse af natriumbicarbonat (NaHCO3). Den molære masse beregnes ved at lægge atommasserne af dets atomer sammen:
Molær masse af NaHCO3 =(1 × 22,99 g/mol) + (1 × 1,01 g/mol) + (3 × 16,00 g/mol) =84,01 g/mol
3. Beregn nødvendige muldvarpe:
Baseret på molforholdet og den ønskede mængde produkt eller reaktant, beregne antallet af krævede mol bagepulver.
4. Konverter mol til masse:
Multiplicer antallet af mol bagepulver med dens molære masse for at opnå den nødvendige masse af bagepulver.
Husk, nøjagtige beregninger afhænger af den specifikke kemiske reaktion og de ønskede resultater. Dobbelttjek altid dine beregninger og se relevante kilder eller vejledninger for at sikre korrekthed.
 Varme artikler
Varme artikler
-
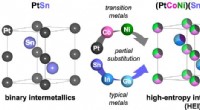 Carbonneutraliserende propylenproduktion katalyserer ændringer i petrokemisk teknikPlatin (Pt) og tin (Sn) steder i intermetallisk PtSn er delvist substitueret med henholdsvis Cobalt og nikkel (Co/Ni) og Indium og Gallium (In/Ga), hvilket danner en PtSn-type højentropi intermetallis
Carbonneutraliserende propylenproduktion katalyserer ændringer i petrokemisk teknikPlatin (Pt) og tin (Sn) steder i intermetallisk PtSn er delvist substitueret med henholdsvis Cobalt og nikkel (Co/Ni) og Indium og Gallium (In/Ga), hvilket danner en PtSn-type højentropi intermetallis -
 Fysikere forklarer, hvordan store sfæriske vira dannesSiyu Li (til venstre) er kandidatstuderende i laboratoriet hos Roya Zandi, en professor i fysik ved UC Riverside. De ses her holde forskellige icosahedral strukturer. Kredit:I. Pittalwala, UC Riversid
Fysikere forklarer, hvordan store sfæriske vira dannesSiyu Li (til venstre) er kandidatstuderende i laboratoriet hos Roya Zandi, en professor i fysik ved UC Riverside. De ses her holde forskellige icosahedral strukturer. Kredit:I. Pittalwala, UC Riversid -
 Kemikere opnår gennembrud i produktionen af tredimensionelle molekylære strukturerKemikere bruger denne eksperimentelle opsætning til fotokemiske reaktioner. Kredit:Peter Bellotti Et vigtigt mål for organisk og medicinsk kemi i de seneste årtier har været den hurtige syntese af
Kemikere opnår gennembrud i produktionen af tredimensionelle molekylære strukturerKemikere bruger denne eksperimentelle opsætning til fotokemiske reaktioner. Kredit:Peter Bellotti Et vigtigt mål for organisk og medicinsk kemi i de seneste årtier har været den hurtige syntese af -
 En dag til at fejre kemiens yndlingsenhed - muldvarpen. Men hvad er en muldvarp?Mole Day er en uofficiel helligdag, der fejres blandt kemikere den 23. oktober, mellem 6:02 og 18:02. Tid og dato er afledt af Avogadros nummer. Kredit:Ekaterina_Minaeva/Shutterstock.com Den 23. o
En dag til at fejre kemiens yndlingsenhed - muldvarpen. Men hvad er en muldvarp?Mole Day er en uofficiel helligdag, der fejres blandt kemikere den 23. oktober, mellem 6:02 og 18:02. Tid og dato er afledt af Avogadros nummer. Kredit:Ekaterina_Minaeva/Shutterstock.com Den 23. o
- Undersøgelse bekræfter høj strålingsmodstand af højentropi-karbidkeramik
- Debunking The Perpetual Motion Myth:Hvad er zero-point energi?
- Setchain, en applikation, der ganges med tusinde af transaktioner pr. minut i enhver blockchain
- Højtemperatursensorteknologier for at øge kraftværkets effektivitet
- En dag på stranden hjælper med at modellere, hvordan lyd bevæger sig gennem kystområder
- Ledere kan lære af at overvåge fjernmedarbejdere under coronavirus


