Hvorfor er ikke-polære forbindelser uopløselige i vand?
Ikke-polære forbindelser er på den anden side molekyler, der ikke har en polær struktur. De har ikke en positiv ende eller en negativ ende, så de er ikke tiltrukket af vandmolekyler. Denne mangel på tiltrækning betyder, at upolære forbindelser ikke opløses i vand.
Et eksempel på en ikke-polær forbindelse er olie. Olie er en blanding af kulbrinter, som er molekyler, der er sammensat af kulstof- og brintatomer. Kulstof- og brintatomer er begge upolære, så olie opløses ikke i vand.
Upolære forbindelsers manglende evne til at opløses i vand er vigtig af en række årsager. En grund er, at det giver os mulighed for at adskille ikke-polære forbindelser fra vand ved hjælp af en proces kaldet ekstraktion. Ekstraktion er en proces, hvor et opløsningsmiddel bruges til at opløse en forbindelse, der ikke er opløselig i vand. Opløsningsmidlet separeres derefter fra vandet, og forbindelsen genvindes.
En anden grund til, at upolære forbindelsers manglende evne til at opløses i vand er vigtig, er, at det hjælper med at opretholde strukturen af levende ting. Levende tings cellemembraner består af et fosfolipid-dobbeltlag, som er et dobbeltlag af fosfolipider. Fosfolipider er molekyler, der har et polært hoved og en upolær hale. Fosfolipidernes polære hoveder vender udad, hvor de interagerer med vand, og de ikke-polære haler vender indad, hvor de interagerer med hinanden. Dette arrangement skaber en barriere, der forhindrer vandopløselige molekyler i at komme ind i cellen og vanduopløselige molekyler i at forlade cellen.
 Varme artikler
Varme artikler
-
 Laserteknikker og fotokemi finder en uhåndgribelig molekylær byggestenMolekyle og skema udlånt af Cheng Zhu og Ralf I. Kaiser. Kredit:Gerd Altmann En vigtig molekylær byggesten i fosforkemi har været uhåndgribelig, indtil nu. University of Hawaii at Manoa forskere h
Laserteknikker og fotokemi finder en uhåndgribelig molekylær byggestenMolekyle og skema udlånt af Cheng Zhu og Ralf I. Kaiser. Kredit:Gerd Altmann En vigtig molekylær byggesten i fosforkemi har været uhåndgribelig, indtil nu. University of Hawaii at Manoa forskere h -
 Effektiv elektrokatalytisk reduktion af nitrat til nitrogen:Lovende måde at fjerne nitrogen fra van…(a-b) SEM-billeder og (c) XRD-mønster af det elektroafsatte Cu2 O tynde film på ramme af Cu-skum; (d) HRTEM-billede af den som fremstillede Cu2 O tynde film. Kredit:Tang Haibin Ifølge et papir for
Effektiv elektrokatalytisk reduktion af nitrat til nitrogen:Lovende måde at fjerne nitrogen fra van…(a-b) SEM-billeder og (c) XRD-mønster af det elektroafsatte Cu2 O tynde film på ramme af Cu-skum; (d) HRTEM-billede af den som fremstillede Cu2 O tynde film. Kredit:Tang Haibin Ifølge et papir for -
 Fanget på fersk gerning:Billeder fanger molekylære bevægelser i realtidForskere afbildede subtile bevægelser af et molekyle kendt som N-methylmorpholin, når det blev exciteret af UV-lys. Kredit:Brown University / SLAC Forskere har brugt ultra-højhastigheds røntgenimp
Fanget på fersk gerning:Billeder fanger molekylære bevægelser i realtidForskere afbildede subtile bevægelser af et molekyle kendt som N-methylmorpholin, når det blev exciteret af UV-lys. Kredit:Brown University / SLAC Forskere har brugt ultra-højhastigheds røntgenimp -
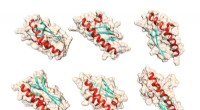 Fødslen af et nyt proteinMulige former for gærproteinet Bsc4, som computeralgoritmen QUARK forudsagde ved kun at bruge proteinets aminosyresekvenser. Kredit:Matthew Cordes, ved hjælp af UCSF Chimera molekylær grafikpakke
Fødslen af et nyt proteinMulige former for gærproteinet Bsc4, som computeralgoritmen QUARK forudsagde ved kun at bruge proteinets aminosyresekvenser. Kredit:Matthew Cordes, ved hjælp af UCSF Chimera molekylær grafikpakke
- Brug af satellitoplysninger til at genopbygge efter en katastrofe
- Brandmyregiftforbindelser kan føre til hudbehandlinger
- ASU Online videnskabskursus bringer liv til en ny måde at undervise på
- Rustbælte-gentrificering og hvordan det gør ondt på de fattige
- Hvordan ændres energien forbundet med bølger, når bølgelængden ændres?
- Elektroingeniør udvikler nye værktøjer i nanoskala til at hjælpe med opdagelser inden for biovid…


