Hvor almindelig er ionbinding i kroppen?
I den menneskelige krop er ionbindinger særligt vigtige for at opretholde proteiners struktur og funktion. Proteiner er store molekyler opbygget af aminosyrer, som er forbundet med peptidbindinger. Peptidbindinger dannes, når carboxylgruppen i en aminosyre reagerer med aminogruppen i en anden aminosyre og frigiver et vandmolekyle. Den resulterende amidbinding er en type kovalent binding, men den har også en vis ionisk karakter på grund af den delvise overførsel af elektroner fra nitrogenatomet til oxygenatomet. Denne delvise ladningsforskel hjælper med at stabilisere proteinmolekylet og giver det mulighed for at folde til sin rette form.
Ionbindinger er også vigtige i funktionen af nukleinsyrer. Nukleinsyrer er polymerer af nukleotider, som består af en nitrogenholdig base, et ribose- eller deoxyribosesukker og en fosfatgruppe. Fosfatgrupperne er negativt ladede, og de interagerer med positivt ladede metalioner for at danne ionbindinger. Disse bindinger hjælper med at stabilisere strukturen af nukleinsyrer og tillader dem at fungere som bærere af genetisk information.
Udover proteiner og nukleinsyrer er ionbindinger også vigtige i kulhydraternes struktur og funktion. Kulhydrater består af monosaccharider, som er simple sukkerarter, der kan bindes sammen for at danne større molekyler. Monosaccharider indeholder både hydroxylgrupper og carbonylgrupper, som begge er polære grupper, der kan deltage i ionbinding. Disse bindinger hjælper med at stabilisere strukturen af kulhydrater og tillader dem at interagere med andre molekyler i kroppen.
Overordnet set er ionbinding en vital kraft i den menneskelige krop, der bidrager til strukturen og funktionen af mange af dens væsentlige molekyler. Uden ionbinding ville kroppen ikke være i stand til at fungere ordentligt og ville sandsynligvis falde fra hinanden.
Sidste artikelHvorfor indeholder læskedrikke opløst kuldioxid?
Næste artikelReagerer metaller med andre metaller?
 Varme artikler
Varme artikler
-
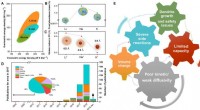 Forskere skitserer den nuværende tilstand af kalium-ion-batteriteknologiPIBs muligheder og udfordringer. (A) sammenligning af LIB, SIB, og PIB med hensyn til energitæthed. (B) overflod af lithium, natrium, og kaliummetal i jordskorpen (vægt%). (C) Stokes radius af Li+, Na
Forskere skitserer den nuværende tilstand af kalium-ion-batteriteknologiPIBs muligheder og udfordringer. (A) sammenligning af LIB, SIB, og PIB med hensyn til energitæthed. (B) overflod af lithium, natrium, og kaliummetal i jordskorpen (vægt%). (C) Stokes radius af Li+, Na -
 Farmakoskopi muliggør opdagelse af immunmodulerende lægemidler ved at analysere immuncelleinterakt…Gregory Vladimer, Nikolaus Krall, Berend Snijder og Giulio Superti-Furga (fra venstre mod højre) er ved siden af Pharmacoscopy high-throughput mikroskop. Kredit:Wolfgang Däuble/CeMM Immunsysteme
Farmakoskopi muliggør opdagelse af immunmodulerende lægemidler ved at analysere immuncelleinterakt…Gregory Vladimer, Nikolaus Krall, Berend Snijder og Giulio Superti-Furga (fra venstre mod højre) er ved siden af Pharmacoscopy high-throughput mikroskop. Kredit:Wolfgang Däuble/CeMM Immunsysteme -
 Video:Kemien bag farveskiftende fugleDit:The American Chemical Society Der er tusindvis af fuglearter her på Jorden, og med de tal følger stor biodiversitet. Fugle er blandt de mest farverige dyr på planeten på grund af de mange for
Video:Kemien bag farveskiftende fugleDit:The American Chemical Society Der er tusindvis af fuglearter her på Jorden, og med de tal følger stor biodiversitet. Fugle er blandt de mest farverige dyr på planeten på grund af de mange for -
 Forskere udvikler en metode til at undersøge millioner af potentielle egenproducerede lægemiddelka…Med en stor samling af fiskekroge, ETH-kemikere forsøger at fange fisken på en meget specifik måde, dvs. et molekylært mål. Kredit:ETH Zürich / Morris Köchle At lede efter nye stoffer er som at fi
Forskere udvikler en metode til at undersøge millioner af potentielle egenproducerede lægemiddelka…Med en stor samling af fiskekroge, ETH-kemikere forsøger at fange fisken på en meget specifik måde, dvs. et molekylært mål. Kredit:ETH Zürich / Morris Köchle At lede efter nye stoffer er som at fi
- Sådan får man succes med mikrobiologi
- 'Frosset adfærd' i ravfossiler:Hvordan man rekonstruerer parringsadfærd for længe uddøde termitt…
- Hvorfor den importerede vaskemaskine, du ønsker, bliver dyrere
- De tre typer vandforurening
- Billede:Hubble fanger supernova-værtsgalaksen
- Private fængsler har en politisk rolle i korrektionsspørgsmål i USA, finder forsker


