Hvad er reaktionen mellem sølvnitrat og aluminiumsulfat?
Den afbalancerede kemiske ligning for reaktionen mellem sølvnitrat og aluminiumsulfat er:
$$3AgNO_3(aq) + Al_2(SO_4)_3(aq) → 3Ag_2SO_4(s) + 2Al(NO_3)_3(aq)$$
I denne reaktion udveksler sølvionerne (Ag+) fra sølvnitrat med aluminiumionerne (Al3+) fra aluminiumsulfat, og nitrationerne (NO3-) fra sølvnitrat udveksles med sulfationerne (SO42-) fra aluminiumsulfat. Produkterne fra reaktionen er sølvsulfat , som er et præcipitat (et fast stof, der dannes, når to opløsninger blandes), og aluminiumnitrat , som er opløseligt i vand.
Den nettoioniske ligning for reaktionen er:
$$2Ag^+ + SO_4^{2-} → Ag_2SO_4(s)$$
Denne ligning viser, at den faktiske reaktion, der sker, er mellem sølvioner (Ag+) og sulfationer (SO42-).
Sidste artikelHvordan beregner man massen af 14,5 mol kobber?
Næste artikelHvad er molmassen af kobber 2?
 Varme artikler
Varme artikler
-
 Små magnetiske partikler gør det muligt for nyt materiale at bøje, vride, og tag fatEt udvalg af genstande fremstillet af polymerer med magnetisk formhukommelse. Kredit:Shuai Wu, Ohio State University Et team af forskere fra Georgia Institute of Technology og Ohio State Universit
Små magnetiske partikler gør det muligt for nyt materiale at bøje, vride, og tag fatEt udvalg af genstande fremstillet af polymerer med magnetisk formhukommelse. Kredit:Shuai Wu, Ohio State University Et team af forskere fra Georgia Institute of Technology og Ohio State Universit -
 Forskere løser det 100-årige metallurgipuslespilFor at forstå præcis, hvordan metaller reagerer på højhastighedskomprimering i molekylære dynamiksimuleringer, LLNL -forskere bruger nye metoder til silikomikroskopi til at afsløre defekter i krystalg
Forskere løser det 100-årige metallurgipuslespilFor at forstå præcis, hvordan metaller reagerer på højhastighedskomprimering i molekylære dynamiksimuleringer, LLNL -forskere bruger nye metoder til silikomikroskopi til at afsløre defekter i krystalg -
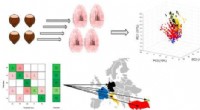 Godkendelse af hasselnøddernes geografiske oprindelseKredit:American Chemical Society Hasselnødder, som olivenolie, ost og andre landbrugsprodukter varierer i smag afhængigt af deres geografiske oprindelse. Fordi forbrugere og processorer er villige
Godkendelse af hasselnøddernes geografiske oprindelseKredit:American Chemical Society Hasselnødder, som olivenolie, ost og andre landbrugsprodukter varierer i smag afhængigt af deres geografiske oprindelse. Fordi forbrugere og processorer er villige -
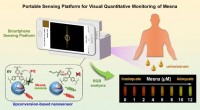 Opkonverteringsbaseret nanosensor udviklet til påvisning af kemoterapilægemidlerFigur 1. Bærbar sensorplatform til visuel kvantitativ overvågning af mesna. Kredit:Hu Bin Som en vigtig regional modgift til at beskytte urinsystemet hos kemoterapipatienter skal mesna (et lægemidd
Opkonverteringsbaseret nanosensor udviklet til påvisning af kemoterapilægemidlerFigur 1. Bærbar sensorplatform til visuel kvantitativ overvågning af mesna. Kredit:Hu Bin Som en vigtig regional modgift til at beskytte urinsystemet hos kemoterapipatienter skal mesna (et lægemidd
- Vulkanudbrud kan forklare Danmarks gigantiske mystiske krystaller
- Ville en bold kastet lodret opad på Venus før eller siden vende tilbage til jorden med samme hasti…
- Ned i kaninhullet:Hvordan elektroner rejser gennem eksotisk nyt materiale
- Hvordan en syndflod af lockdown-frivillige reddede Storbritanniens skjulte vejrhistorie
- Billede:Japansk skærgård og det vestlige Stillehav
- Grafen svamp hjælper litium svovl batterier med at nå nyt potentiale


