Hvad sker der, når du blander to stoffer?
1. Fysiske ændringer:
- Løsning: Et stof (opløst stof) opløses i et andet (opløsningsmiddel) og danner en homogen blanding kaldet en opløsning. De opløste partikler fordeler sig jævnt i opløsningsmidlet, hvilket resulterer i en ensartet sammensætning. Almindelige eksempler omfatter opløsning af sukker i vand eller salt i vand.
- Suspendering: Hvis partiklerne af det ene stof ikke opløses, men forbliver spredt i det andet stof, dannes en suspension. Partiklerne er store nok til til sidst at sætte sig ned på grund af tyngdekraften. Eksempler omfatter mudret vand eller sand i vand.
- Kolloid: Kolloider er blandinger, hvor partiklerne har en mellemstørrelse mellem dem i opløsninger og suspensioner. De virker homogene med det blotte øje, men viser spredning af lys (Tyndall-effekt). Eksempler omfatter mælk, mayonnaise og tåge.
2. Kemiske ændringer (reaktioner):
- Danning af nye forbindelser: Når to eller flere stoffer reagerer kemisk, kan de danne nye forbindelser med forskellige egenskaber. Udgangsstofferne omdannes til nye produkter, og de kemiske bindinger mellem atomer omlejres. Almindelige eksempler omfatter forbrændingsreaktioner (afbrænding af brændstof), syre-base reaktioner og oxidationsreaktioner.
- Udgivelse eller absorption af energi: Kemiske reaktioner kan involvere frigivelse eller absorption af energi i form af varme, lys eller lyd. For eksempel frigiver afbrænding af træ varmeenergi, og eksplosioner frigiver både varme og lydenergi.
3. Ingen reaktion: I nogle tilfælde vil blanding af stoffer muligvis ikke resultere i nogen mærkbare ændringer. Stofferne kan forblive kemisk uændrede og blot blandes fysisk uden at danne nye forbindelser.
4. Faseændringer:
- Smeltning og frysning: Blanding af stoffer med forskellige smeltepunkter kan resultere i faseændringer. Tilførsel af varme kan smelte et fast stof (såsom is) til en væske, mens afkøling kan få en væske (såsom vand) til at fryse til et fast stof.
- Kogning og kondensering: Tilsvarende kan blanding af stoffer med forskellige kogepunkter føre til faseændringer. Væsker med lavere kogepunkter kan fordampe, mens dampe eller gasser kan kondensere og danne væsker, når temperaturen eller trykket ændres.
Det specifikke resultat ved blanding af to stoffer afhænger af deres kemiske egenskaber, koncentrationer, temperatur, tryk og andre faktorer. Det er afgørende at forstå de involverede stoffers egenskaber og potentielle reaktivitet for at forudsige resultatet nøjagtigt.
Sidste artikelEgenskaber, der afhænger af stoffernes reaktion med andre stoffer?
Næste artikelEr masse og volumen en kemisk egenskab?
 Varme artikler
Varme artikler
-
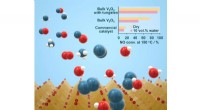 Wolframsubstitueret vanadiumoxid indånder frisk luft i katalysatorteknologiIllustration af ammoniak og nitrogenoxidmolekyler over et krystallinsk katalytisk materiale. (indsat) Kvælstofoxidkonverteringshastigheder ved 150 grader Celsius for wolframsubstitueret bulkvanadiumox
Wolframsubstitueret vanadiumoxid indånder frisk luft i katalysatorteknologiIllustration af ammoniak og nitrogenoxidmolekyler over et krystallinsk katalytisk materiale. (indsat) Kvælstofoxidkonverteringshastigheder ved 150 grader Celsius for wolframsubstitueret bulkvanadiumox -
 Forskere forvandler akvakulturaffald til nyt biomateriale til vævsreparationForskerne mener, at biomaterialet er et lovende alternativ til den nuværende standardpraksis med at bruge en patients eget væv, hvilket kræver yderligere operation til knogleudtrækning. På samme tid,
Forskere forvandler akvakulturaffald til nyt biomateriale til vævsreparationForskerne mener, at biomaterialet er et lovende alternativ til den nuværende standardpraksis med at bruge en patients eget væv, hvilket kræver yderligere operation til knogleudtrækning. På samme tid, -
 Billigere brintbrændselscelle kan betyde bedre grønne energimulighederBrændselscellen bliver testet i laboratoriet. Kredit:Imperial College London Brintbrændselsceller omdanner brint til elektricitet med vanddamp som det eneste biprodukt, hvilket gør dem til et attra
Billigere brintbrændselscelle kan betyde bedre grønne energimulighederBrændselscellen bliver testet i laboratoriet. Kredit:Imperial College London Brintbrændselsceller omdanner brint til elektricitet med vanddamp som det eneste biprodukt, hvilket gør dem til et attra -
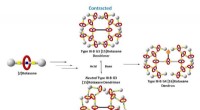 Gennembrud i makromolekylære maskiner til aktivt kontrolleret levering af kræftmedicinMolekylære maskiners kemiske struktur. Kredit:HKBU Forskere fra Hong Kong Baptist University (HKBU) demonstrerede design og syntese af et smart globulært makromolekylært maskinkøretøj til aktivt k
Gennembrud i makromolekylære maskiner til aktivt kontrolleret levering af kræftmedicinMolekylære maskiners kemiske struktur. Kredit:HKBU Forskere fra Hong Kong Baptist University (HKBU) demonstrerede design og syntese af et smart globulært makromolekylært maskinkøretøj til aktivt k
- Tidevandshaler opdaget omkring dværggalaksen DDO 44
- Overbelastningspriser, socialt boligbyggeri, og en bæredygtig New York City
- 'Leaveisme' og 'tilstedeværelse' fortsætter, selv når arbejdsgiverne er mere fleksible. Sådan bl…
- Silkefibre kan være højteknologiske naturlige metamaterialer
- Et sting i tiden:Hvordan en kvantefysiker opfandt ny kode fra gamle tricks
- Bindemiddelfri MWW-type titanosilikat til selektiv og holdbar propylenepoxidering


