Hvad sker der, når du opvarmer glycerol med kaliumdichromat?
2CH2OH-CHOH-CH2OH + K2Cr2O7 + H2SO4 → 3CO2 + Cr2(SO4)3 + K2SO4 + H2O
I denne reaktion oxideres glycerolmolekylerne for at producere kuldioxid (CO2) og vand (H2O). I mellemtiden reduceres kaliumdichromatet fra +6-oxidationstilstanden i Cr2O72- til +3-oxidationstilstanden i Cr3+. Svovlsyren (H2SO4) tjener som katalysator for reaktionen.
Reaktionen er meget eksoterm og frigiver en betydelig mængde varme. Dette skyldes, at oxidationen af glycerol er en yderst gunstig proces, og den energi, der frigives fra reaktionen, er i form af varme. Derudover bidrager nedbrydningen af kaliumdichromat også til varmeafgivelsen.
Samlet set er reaktionen mellem glycerol og kaliumdichromat et klassisk eksempel på en oxidations-reduktionsreaktion, hvor den ene art oxideres (glycerol), mens den anden reduceres (kaliumdichromat). Reaktionen producerer kuldioxid, vand, chromsulfat og kaliumsulfat sammen med frigivelsen af en betydelig mængde varme.
Sidste artikelHvilken slags binding finder sted i NaOH?
Næste artikelHvad er formelmassen af S2Cl2?
 Varme artikler
Varme artikler
-
 Forskning ser på materialets friktionsegenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuum tribometer brugt til friktions- og slidtest, som er blandt de væ
Forskning ser på materialets friktionsegenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuum tribometer brugt til friktions- og slidtest, som er blandt de væ -
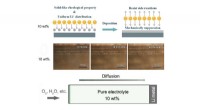 Hydrofob silica kolloid elektrolyt lover sikrere lithium-oxygen batterierSkematisk graf og eksperimentelle data, der viser den lithiumdendritforebyggende effekt af 10 vægt% HSCE. Skematisk graf og eksperimentelle data, der viser antikorrosionseffekten af 10 vægt% HSCE. K
Hydrofob silica kolloid elektrolyt lover sikrere lithium-oxygen batterierSkematisk graf og eksperimentelle data, der viser den lithiumdendritforebyggende effekt af 10 vægt% HSCE. Skematisk graf og eksperimentelle data, der viser antikorrosionseffekten af 10 vægt% HSCE. K -
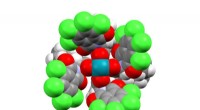 Ny katalysator styrer aktiveringen af en carbon-hydrogenbindingDirhodium (vist med blåt) driver reaktionen, mens formen på stilladset omkring det styrer hvilken CH-binding katalysatoren virker på. Kredit:Kuangbiao Liao, Emory Universitet. Kemikere har udvikle
Ny katalysator styrer aktiveringen af en carbon-hydrogenbindingDirhodium (vist med blåt) driver reaktionen, mens formen på stilladset omkring det styrer hvilken CH-binding katalysatoren virker på. Kredit:Kuangbiao Liao, Emory Universitet. Kemikere har udvikle -
 Enkeltcelletest kan afsløre præcis, hvordan lægemidler dræber kræftcellerD 2 O-probet CANcer-følsomhedstest Ramanometri (D 2 O-CANST-R) Kredit:LIU Yang Kræftceller er smarte, når det kommer til medicin mod kræft, udvikler sig og bliver resistente over for selv de s
Enkeltcelletest kan afsløre præcis, hvordan lægemidler dræber kræftcellerD 2 O-probet CANcer-følsomhedstest Ramanometri (D 2 O-CANST-R) Kredit:LIU Yang Kræftceller er smarte, når det kommer til medicin mod kræft, udvikler sig og bliver resistente over for selv de s
- Elon Musk siger, at han forlader rådgivende paneler i Det Hvide Hus
- Mikrobrygning går mere mikro
- Et gennembrud i estimering af størrelsen af et (for det meste skjult) netværk
- De første rumbagte småkager tog to timer i eksperimentel ovn
- Den utrolige hastighed for elektronemission fra et atom
- Ny lyddiffusor er ti gange tyndere end eksisterende designs


