Hvorfor ekstraheres natriumbenzoat let til H20, mens original benzoesyre ikke H20?
Benzoesyre er en svag syre med en pKa på 4,2. Det betyder, at det kun delvist dissocierer i vand, og de fleste af molekylerne forbliver i deres udissocierede form. De udissocierede molekyler er ikke særlig opløselige i vand, fordi de er upolære.
Natriumbenzoat er på den anden side et stærkt salt, der dissocierer fuldstændigt i vand. Natriumionerne og benzoationerne er begge meget opløselige i vand, fordi de er polære. Benzoationerne kan danne brintbindinger med vandmolekylerne, hvilket gør dem endnu mere opløselige.
Som et resultat er natriumbenzoat meget mere opløseligt i vand end benzoesyre. Denne forskel i opløselighed er vigtig for ekstraktion af benzoesyre fra vandige opløsninger. Benzoesyre kan ekstraheres i et organisk opløsningsmiddel, såsom diethylether, ved at tilsætte natriumhydroxid til den vandige opløsning. Natriumhydroxidet vil omdanne benzoesyren til natriumbenzoat, som derefter ekstraheres i det organiske opløsningsmiddel.
 Varme artikler
Varme artikler
-
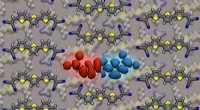 Tuning the energy gap:En ny tilgang til organiske halvledereVarierende forholdet mellem 3T -molekyler (forgrund) og 6T -molekyler (angivet i baggrunden) i blandingen gør det muligt at afstemme hullet kontinuerligt. Kredit:Sebastian Hutsch, Frank Ortmann Tu
Tuning the energy gap:En ny tilgang til organiske halvledereVarierende forholdet mellem 3T -molekyler (forgrund) og 6T -molekyler (angivet i baggrunden) i blandingen gør det muligt at afstemme hullet kontinuerligt. Kredit:Sebastian Hutsch, Frank Ortmann Tu -
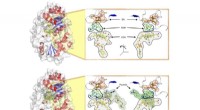 Hvordan et bestemt protein regulerer op til to tredjedele af verdens metanudledningOverfladeillustrationer af enzymet Mmp10, der viser (øverst) proteinet med det komplette sæt af co-faktorer, der kræves for at den enzymatiske reaktion kan forekomme (nemlig:SF4-klyngen, SAM og cobala
Hvordan et bestemt protein regulerer op til to tredjedele af verdens metanudledningOverfladeillustrationer af enzymet Mmp10, der viser (øverst) proteinet med det komplette sæt af co-faktorer, der kræves for at den enzymatiske reaktion kan forekomme (nemlig:SF4-klyngen, SAM og cobala -
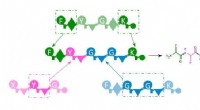 Nye aktive ingredienser fra værktøjskassenSkematisk diagram af værktøjskassesystemet af NRPS-enzymer til produktion af nye aktive ingredienser. Fragmenter fra naturlige systemer (grøn, magenta, blå) samles igen i en ny rækkefølge (midten) og
Nye aktive ingredienser fra værktøjskassenSkematisk diagram af værktøjskassesystemet af NRPS-enzymer til produktion af nye aktive ingredienser. Fragmenter fra naturlige systemer (grøn, magenta, blå) samles igen i en ny rækkefølge (midten) og -
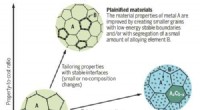 Plainification lover at forbedre materielle bæredygtighedMaterialernes ydeevne forbedres ofte ved at stabilisere grænseflader mellem korn ved at legere med andre elementer. (Billede af SYNL) Omfattende legering gør materialeudvikling mere afhængig af kn
Plainification lover at forbedre materielle bæredygtighedMaterialernes ydeevne forbedres ofte ved at stabilisere grænseflader mellem korn ved at legere med andre elementer. (Billede af SYNL) Omfattende legering gør materialeudvikling mere afhængig af kn
- Træplantning har potentiale til at øge kulstofbindingskapaciteten
- Sådan fungerer molekylær gastronomi
- W. M. Keck Observatory opnår første lys med nyt instrument
- Ingeniører udtænker en ny metode til at fjerne skadelige E. coli fra vand
- Hvor mange mg er der i 0,2 g?
- Nanoreaktorstrategi genererer overlegne understøttede bimetalliske katalysatorer


