Hvorfor opløses opløsningen af hvidt bundfald Zinkhydroxid i overskud af ammoniumhydroxid?
Når overskydende ammoniumhydroxid tilsættes til zinkhydroxidpræcipitatet, reagerer hydroxidionerne fra ammoniumhydroxid med zinkionerne for at producere zinkhydroxid. Imidlertid kan det overskydende ammoniumhydroxid derefter reagere med zinkhydroxidet og danne tetraamminezink(II)-ionen. Denne komplekse ion er opløselig i vand, hvorfor det hvide bundfald opløses, når overskydende ammoniumhydroxid tilsættes.
Reaktionen mellem zinkhydroxid og ammoniumhydroxid kan repræsenteres som følger:
Zn(OH)2(s) + 4NH4OH(aq) -> [Zn(NH3)4]2+(aq) + 4H2O(l)
Tetraamminezinc(II)-ionen er en stabil kompleks ion, fordi den har et højt ladnings-til-størrelse-forhold. Det betyder, at zinkionens positive ladning er jævnt fordelt over de fire ammoniakmolekyler, hvilket gør den mindre tilbøjelig til at reagere med andre ioner i opløsningen.
Sidste artikelHvilke kemikalier bruges til at lave en skummadras?
Næste artikelEr aluminiumsfolie skåret i halve kemisk eller fysisk?
 Varme artikler
Varme artikler
-
 Skeder driver kraftfulde nye kunstige musklerDenne illustration viser et snoet carbon nanorør-garn (CNT) (venstre) og en kappedrevet kunstig muskel (SRAM) fremstillet ved at belægge et snoet CNT-garn med en polymerskede. Et scanningselektronmikr
Skeder driver kraftfulde nye kunstige musklerDenne illustration viser et snoet carbon nanorør-garn (CNT) (venstre) og en kappedrevet kunstig muskel (SRAM) fremstillet ved at belægge et snoet CNT-garn med en polymerskede. Et scanningselektronmikr -
 3-D print med applikationer i den farmaceutiske industriKredit:CC0 Public Domain University of Sevilla forskere, i samarbejde med University of Nottingham, har formået at skabe det første billede af nanopartikler af stabiliseret guld med biologisk nedb
3-D print med applikationer i den farmaceutiske industriKredit:CC0 Public Domain University of Sevilla forskere, i samarbejde med University of Nottingham, har formået at skabe det første billede af nanopartikler af stabiliseret guld med biologisk nedb -
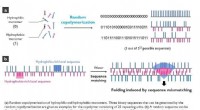 Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l
Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l -
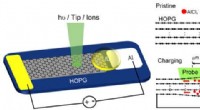 Overfladeeffekt af elektroder afsløret ved operando overfladevidenskabelige metoderSkematisk af Al/HOPG planar batteri. Kredit:@Science China Press Overflade og grænseflade spiller en afgørende rolle i energilagringsenheder, kræver derfor in-situ/operando-metoder til at sonde de
Overfladeeffekt af elektroder afsløret ved operando overfladevidenskabelige metoderSkematisk af Al/HOPG planar batteri. Kredit:@Science China Press Overflade og grænseflade spiller en afgørende rolle i energilagringsenheder, kræver derfor in-situ/operando-metoder til at sonde de
- Rapport identificerer store udfordringer for bedre at forberede sig på vulkanudbrud
- NASA rykker op på den første kvindelige rumvandring for at reparere enheden
- Styrke fra evig sorg:Hvordan aboriginerne oplever bushbrandkrisen
- Hvordan bevæger lyd sig i vibrationer?
- Brug af vandmolekyler til at låse op for neurons hemmeligheder
- En lovende metode til at producere fiberbatterier i industriel skala


