Hvad er pH i opløsningen, hvis hydroxid i koncentration 4?
$$pH =14 - pOH$$
Hvor pOH er den negative logaritme af hydroxidionkoncentrationen:
$$pOH =-\log[OH^-]$$
Givet [OH^-] =4:
$$pOH =-\log(4) =0,602$$
Substitution af pOH i pH-formlen:
$$pH =14 - 0,602 =13,398$$
Derfor er opløsningens pH ca. 13,398.
 Varme artikler
Varme artikler
-
 Bekræftelse af stamtavlen for urankuber fra Nazitysklands mislykkede atomprogramRobertson med PNNLs terning, som er i et beskyttende etui. Kredit:Andrea Starr/PNNL Under Anden Verdenskrig, Nazityskland og USA var kapløb om at udvikle nuklear teknologi. Før Tyskland kunne lykk
Bekræftelse af stamtavlen for urankuber fra Nazitysklands mislykkede atomprogramRobertson med PNNLs terning, som er i et beskyttende etui. Kredit:Andrea Starr/PNNL Under Anden Verdenskrig, Nazityskland og USA var kapløb om at udvikle nuklear teknologi. Før Tyskland kunne lykk -
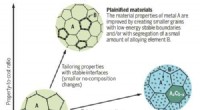 Plainification lover at forbedre materielle bæredygtighedMaterialernes ydeevne forbedres ofte ved at stabilisere grænseflader mellem korn ved at legere med andre elementer. (Billede af SYNL) Omfattende legering gør materialeudvikling mere afhængig af kn
Plainification lover at forbedre materielle bæredygtighedMaterialernes ydeevne forbedres ofte ved at stabilisere grænseflader mellem korn ved at legere med andre elementer. (Billede af SYNL) Omfattende legering gør materialeudvikling mere afhængig af kn -
 Algoritme bruger massespektrometridata til at forudsige molekylernes identitetKredit:Pixabay/CC0 Public Domain En algoritme designet af forskere fra Carnegie Mellon Universitys Computational Biology Department og St. Petersburg State University i Rusland kunne hjælpe videns
Algoritme bruger massespektrometridata til at forudsige molekylernes identitetKredit:Pixabay/CC0 Public Domain En algoritme designet af forskere fra Carnegie Mellon Universitys Computational Biology Department og St. Petersburg State University i Rusland kunne hjælpe videns -
 Størrelse betyder noget, når det kommer til atomare egenskaberEn illustration af kaliumatomer, der undergår ændringer i fundamentale egenskaber såsom radius, energi og elektronegativitet, da de komprimeres af omgivende neonatomer Kredit:Neuroncollective, Daniel
Størrelse betyder noget, når det kommer til atomare egenskaberEn illustration af kaliumatomer, der undergår ændringer i fundamentale egenskaber såsom radius, energi og elektronegativitet, da de komprimeres af omgivende neonatomer Kredit:Neuroncollective, Daniel
- Behandling af afhængighed:Cryo-EM-teknologien muliggør det umulige
- Spanien sætter temperaturrekorder, Storbritannien ser den varmeste dag i 2020
- Indeholder en fosfatgruppe fosfor?
- "The Silverback Gorillas Diet
- Hvad er reaktionen for aluminium og oxygen?
- Oxidlag øger ydeevnen i kvantepriksolceller med nanotråd


