Hvad er virkningerne af temperatur- og volumengasprøver ved konstant tryk?
Effekter af temperatur på en gasprøve ved konstant tryk:
1. Lydstyrkeudvidelse :Når temperaturen på en gas stiger, stiger dens partiklers gennemsnitlige kinetiske energi. Dette får partiklerne til at bevæge sig hurtigere og kollidere hyppigere med beholdervæggene, hvilket udøver større tryk. For at opretholde konstant tryk skal beholderen udvide sig, så gaspartiklerne får mere plads til at bevæge sig.
2. Lydstyrkesammentrækning :Omvendt, hvis temperaturen falder, falder den gennemsnitlige kinetiske energi af gaspartiklerne. Dette fører til langsommere partikelbevægelse, reducerede kollisioner med beholdervæggene og lavere tryk. For at opretholde konstant tryk skal beholderen trække sig sammen, hvilket reducerer den tilgængelige plads til gaspartiklerne.
3. Lineært forhold :Charles's Lov siger, at volumenet af en gas er direkte proportional med dens temperatur, når trykket forbliver konstant. Denne sammenhæng kan udtrykkes matematisk som V ∝ T, hvor V repræsenterer gassens volumen, T repræsenterer temperaturen, og symbolet ∝ angiver proportionalitet.
4. Absolut nul :Når temperaturen nærmer sig det absolutte nulpunkt (0 Kelvin eller -273,15 grader Celsius), når volumenet af en gas teoretisk sin minimumsværdi under forudsætning af ideel gasadfærd. Ved denne temperatur har gaspartiklerne den lavest mulige kinetiske energi, og deres bevægelse ophører praktisk talt.
Sammenfattende, når temperaturen stiger, stiger volumenet af en gasprøve proportionalt, mens når temperaturen falder, falder volumenet proportionalt under forudsætning af konstant tryk. Dette forhold er grundlæggende for forståelsen af gassers adfærd og har praktiske anvendelser på forskellige områder, såsom gaslagring, termiske ekspansionsanordninger og vejrballoner
Sidste artikelHvad er scolar-mængder?
Næste artikelHvordan påvirker tryktemperaturen og antallet af partikler en gass adfærd?
 Varme artikler
Varme artikler
-
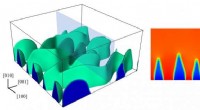 Ikke så hurtigt:Nogle batterier kan skubbes for langtTil venstre, en 3D-model af Rice Universitys materialeforskere viser en fasegrænse, da en delithierende lithiumjernphosphatkatode undergår hurtig afladning. Til højre, et tværsnit viser den fingerlign
Ikke så hurtigt:Nogle batterier kan skubbes for langtTil venstre, en 3D-model af Rice Universitys materialeforskere viser en fasegrænse, da en delithierende lithiumjernphosphatkatode undergår hurtig afladning. Til højre, et tværsnit viser den fingerlign -
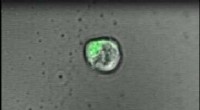 Forskere fremmer oprettelsen af kunstig lymfeknude til bekæmpelse af kræft, andre sygdommeT-celler interagerer med den transparente gel. Kredit:Hawley Pruitt I et principbeskyttet studie på mus, forskere ved Johns Hopkins Medicine rapporterer oprettelsen af en specialiseret gel, der
Forskere fremmer oprettelsen af kunstig lymfeknude til bekæmpelse af kræft, andre sygdommeT-celler interagerer med den transparente gel. Kredit:Hawley Pruitt I et principbeskyttet studie på mus, forskere ved Johns Hopkins Medicine rapporterer oprettelsen af en specialiseret gel, der -
 Svampe, fjer kombineres i biologisk nedbrydelige skoTo University of Delaware-studerende har lavet en biologisk nedbrydelig sko ved hjælp af svampe, kyllingefjer og tekstilaffald. Prototypeskoen består af en myceliumbaseret sål, dækket med vegansk læde
Svampe, fjer kombineres i biologisk nedbrydelige skoTo University of Delaware-studerende har lavet en biologisk nedbrydelig sko ved hjælp af svampe, kyllingefjer og tekstilaffald. Prototypeskoen består af en myceliumbaseret sål, dækket med vegansk læde -
 Retsmedicinsk forskning viser, at tekstilfibre kan overføres mellem tøj uden kontaktKredit:CC0 Public Domain Banebrydende retsmedicinsk forskning ved Northumbria University, Newcastle, har for første gang afsløret, at tekstilfibre kan, under visse omstændigheder, flyttes mellem t
Retsmedicinsk forskning viser, at tekstilfibre kan overføres mellem tøj uden kontaktKredit:CC0 Public Domain Banebrydende retsmedicinsk forskning ved Northumbria University, Newcastle, har for første gang afsløret, at tekstilfibre kan, under visse omstændigheder, flyttes mellem t
- Humanoid Atlas får lidt luft og jogger, springer over log
- Måneturister risikerer hård tur, siger eksperter
- Hvad er den bølge, der overfører energi gennem det tomme rum?
- Økonomisk sværvægter Boeing hamret af dobbelte kriser
- Sjov eksploderende videnskabseksperimenter
- Hvor mange prikker skal tegnes i Lewis prikstrukturen for et oxygenatom?


