Hvad er navnet på ion i ammoniakopløsning, der forårsager pH 10?
Reaktionen, der opstår, når ammoniak opløses i vand, er som følger:
NH3 + H2O ⇌ NH4+ + OH-
I denne reaktion reagerer ammoniakmolekyle med vand for at danne ammoniumioner NH4+ og hydroxidioner OH-. Tilstedeværelsen af hydroxidioner i opløsningen øger dens pH, hvilket gør den mere basisk.
For en opløsning med en pH på 10 ved stuetemperatur kan koncentrationen af hydroxidioner [OH-] beregnes ved hjælp af følgende formel:
[OH-] =10^(-pH) =10^(-10) M =1 x 10^-10 M
Derfor er hydroxidionerne (OH-) i en ammoniakopløsning med en pH på 10 ansvarlige for opløsningens basiske natur og høje pH.
 Varme artikler
Varme artikler
-
 Hvorfor løg får os til at græde (og hvorfor nogle ikke gør det)Kredit:Shutterstock Mark Anthony i Shakespeares Cleopatra kan have henvist til tårerne, der lever i løget. Men hvorfor får løg os egentlig til at græde? Og hvorfor er det kun nogle løg, der får os
Hvorfor løg får os til at græde (og hvorfor nogle ikke gør det)Kredit:Shutterstock Mark Anthony i Shakespeares Cleopatra kan have henvist til tårerne, der lever i løget. Men hvorfor får løg os egentlig til at græde? Og hvorfor er det kun nogle løg, der får os -
 Et afstembart 2D kovalent netværk til ladningsselektiv fjernelse af giftige farvestoffer fra spilde…Kredit:Khalifa University Syntetiske farvestoffer er almindelige ingredienser i tekstilindustrien, men på grund af deres generelle brug, de finder ofte vej til vandområder fra industrispildevand,
Et afstembart 2D kovalent netværk til ladningsselektiv fjernelse af giftige farvestoffer fra spilde…Kredit:Khalifa University Syntetiske farvestoffer er almindelige ingredienser i tekstilindustrien, men på grund af deres generelle brug, de finder ofte vej til vandområder fra industrispildevand, -
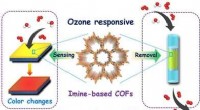 Krystallinske polymerer til hurtig påvisning og effektiv nedbrydning af ozonKredit:Wiley Ozon er et problematisk luftforurenende stof, der forårsager alvorlige helbredsproblemer. Et nyudviklet materiale indikerer ikke kun hurtigt og selektivt tilstedeværelsen af ozon, m
Krystallinske polymerer til hurtig påvisning og effektiv nedbrydning af ozonKredit:Wiley Ozon er et problematisk luftforurenende stof, der forårsager alvorlige helbredsproblemer. Et nyudviklet materiale indikerer ikke kun hurtigt og selektivt tilstedeværelsen af ozon, m -
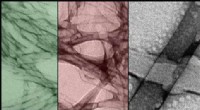 Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen
Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen
- Klimamodellering viser betydelige ændringer i kystskove i det nordvestlige Stillehav i det nordvest…
- Opstart af bioteknologi rejser $ 64 millioner til at slette kræft, selv i navnet
- Ny maskinlæringsalgoritme kan forudsige alder og køn fra kun din Twitter-profil
- Ny enhed opdager hurtigt skadelige bakterier i blodet
- Metal nanopartikler til billeddiagnostik guidet fototerapi
- Ny fiberbaseret sensor kunne hurtigt opdage strukturelle problemer i broer og dæmninger


