Hvad er korrekt med hensyn til reaktionen mellem kaliumferrocyanid og KMnO4 i sur opløsning Permanganation er oxidationsmiddel eller oxideret?
Forklaring:
I reaktionen mellem kaliumferrocyanid og KMnO4 i sur opløsning fungerer permanganationen (MnO4-) som oxidationsmiddel. Det gennemgår reduktion og accepterer elektroner fra ferrocyanid-ionen (Fe(CN)64-), som oxideres i processen. Den afbalancerede kemiske ligning for reaktionen er:
2KMnO4 + 10Fe(CN)64- + 8H+ → 2Mn2+ + 10Fe(CN)63- + 5H2O
I denne reaktion reduceres permanganationen (MnO4-) fra en oxidationstilstand på +7 til en oxidationstilstand på +2, mens ferrocyanidionen (Fe(CN)64-) oxideres fra en oxidationstilstand på +2 til en oxidationstilstand på +3.
Sidste artikelEr H1.9O1.9 en formel for forbindelse?
Næste artikelHvordan syrnet kaliumpermanganat bruges som reduktionsreagens?
 Varme artikler
Varme artikler
-
 Varmeledende plastik kan føre til lettere elektronik, bilerHøj varmeledningsevne i tynde polyelektrolytfilm via kontrolleret ionisering. Kredit: Videnskab fremskridt (2017). DOI:10.1126/sciadv.1700342 Avanceret plast kan indføre lettere, billigere, mere
Varmeledende plastik kan føre til lettere elektronik, bilerHøj varmeledningsevne i tynde polyelektrolytfilm via kontrolleret ionisering. Kredit: Videnskab fremskridt (2017). DOI:10.1126/sciadv.1700342 Avanceret plast kan indføre lettere, billigere, mere -
 Forskere forbedrer katalysatoren, der ødelægger kemikalier for evigt med sollysIllustration, der viser, hvordan et kompositmateriale indeholdende plader af bornitrid (gitter af blå og sølvkugler) og nanopartikler af titaniumdioxid (grå kugler) bruger langbølget ultraviolet energ
Forskere forbedrer katalysatoren, der ødelægger kemikalier for evigt med sollysIllustration, der viser, hvordan et kompositmateriale indeholdende plader af bornitrid (gitter af blå og sølvkugler) og nanopartikler af titaniumdioxid (grå kugler) bruger langbølget ultraviolet energ -
 Et stof, mange sygdommeKredit:CC0 Public Domain Det virker for godt til at være sandt:et enkelt stof, der kunne behandle menneskehedens værste lidelser, herunder åreforkalkning, Kræft, Alzheimers, Parkinsons og gigt. Al
Et stof, mange sygdommeKredit:CC0 Public Domain Det virker for godt til at være sandt:et enkelt stof, der kunne behandle menneskehedens værste lidelser, herunder åreforkalkning, Kræft, Alzheimers, Parkinsons og gigt. Al -
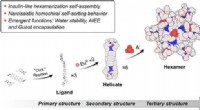 Hexameriske lanthanid-organiske kapsler med tertiær struktur, nye funktionerKredit: Journal of the American Chemical Society (2021). DOI:10.1021/jacs.1c01168 Metalrettede samlinger er blevet en meget brugt tilgang til at designe sofistikerede og multifunktionelle kunstig
Hexameriske lanthanid-organiske kapsler med tertiær struktur, nye funktionerKredit: Journal of the American Chemical Society (2021). DOI:10.1021/jacs.1c01168 Metalrettede samlinger er blevet en meget brugt tilgang til at designe sofistikerede og multifunktionelle kunstig
- Sådan finder du længden på siderne af en ottekant Baseret på Diameter
- Forskere kvantificerer verdensomspændende tab af fosfor på grund af jorderosion for første gang
- Hvor længe observeres solnedgange typisk at vare?
- Blandede nanopartikelsystemer kan hjælpe med at rense vand og generere brint
- Bioinspiration-planteinspirerede pipetter
- Hvad er fluorescerende lysets spektrum?


