Hvad bestemmer et stofs kogepunkt?
Et stofs kogepunkt bestemmes af flere faktorer, herunder:
* Intermolekylære kræfter: Styrken af de intermolekylære kræfter mellem et stofs molekyler påvirker dets kogepunkt. Stoffer med stærke intermolekylære kræfter, såsom hydrogenbinding, har højere kogepunkter end stoffer med svage intermolekylære kræfter, såsom van der Waals-kræfter.
* Molekylvægt: Et stofs molekylvægt påvirker også dets kogepunkt. Stoffer med højere molekylvægt har højere kogepunkter end stoffer med lavere molekylvægt. Dette skyldes, at tungere molekyler har flere intermolekylære kræfter imellem sig.
* Tryk: Det omgivende miljøs tryk påvirker også et stofs kogepunkt. Jo højere tryk, jo højere kogepunkt. Det skyldes, at det øgede tryk gør det sværere for stoffets molekyler at slippe ud af væskefasen.
Et stofs kogepunkt er en karakteristisk egenskab, som kan bruges til at identificere stoffet. Det er også en vigtig faktor i mange kemiske processer, såsom destillation og fordampning.
 Varme artikler
Varme artikler
-
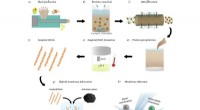 Dekontaminering af tungmetalvand ved hjælp af protein fra planteaffaldSkematisk over procesflow fra plantefrø til den amyloidbaserede filtreringsmembran. a) Fremstilling af solsikke- og jordnøddemel ved skruepresning af frø. b) Vandig proteinekstraktion af måltider (bru
Dekontaminering af tungmetalvand ved hjælp af protein fra planteaffaldSkematisk over procesflow fra plantefrø til den amyloidbaserede filtreringsmembran. a) Fremstilling af solsikke- og jordnøddemel ved skruepresning af frø. b) Vandig proteinekstraktion af måltider (bru -
 Registrering af skadelige molekyler med lysLysbølger, der bevæger sig på isolerende eller dielektriske materialer, såsom glas, kan øge følsomheden for optiske sensorer og kan være tilgængelige kommercielt inden for få år. Kredit:andreadonetti
Registrering af skadelige molekyler med lysLysbølger, der bevæger sig på isolerende eller dielektriske materialer, såsom glas, kan øge følsomheden for optiske sensorer og kan være tilgængelige kommercielt inden for få år. Kredit:andreadonetti -
 Grønnere kemi gennem ny tilgang til katalyseKun 30 mg af den nye katalysator er nødvendig for at omdanne 1 kg substrat. Kredit:TU Delft/Wenjun Yang Forskere ved Delft University of Technology (TU Delft) har udviklet en katalysator, der er e
Grønnere kemi gennem ny tilgang til katalyseKun 30 mg af den nye katalysator er nødvendig for at omdanne 1 kg substrat. Kredit:TU Delft/Wenjun Yang Forskere ved Delft University of Technology (TU Delft) har udviklet en katalysator, der er e -
 Overflade oxygenerede arter forbedrer kobolt-katalyseret Fischer-Tropsch-synteseReduktionsprocessen for koboltarter og oprindelsen til den forbedrede iboende aktivitet. Kredit:JIANG Qian Carbid-understøttede metalkatalysatorer er lovende på grund af metalcarbids særlige egens
Overflade oxygenerede arter forbedrer kobolt-katalyseret Fischer-Tropsch-synteseReduktionsprocessen for koboltarter og oprindelsen til den forbedrede iboende aktivitet. Kredit:JIANG Qian Carbid-understøttede metalkatalysatorer er lovende på grund af metalcarbids særlige egens
- Vores energisult er knyttet til vores økonomiske fortid:undersøgelse
- Afklaring af kaoset i narhvaladfærd
- Sådan køres din køleskab med solenergi
- Hvordan Europas skove regenererer – uden menneskelig indblanding
- Hvordan ved du, hvor vulkansk aske ender?
- Musik var en form for modstand for kvinder under Civil Rights Movement


