Hvad bemærker du ved antallet af valenselektroner, når de bevæger sig fra venstre mod højre over en række eller et punktum i det periodiske system na-mg-al-si-p-s-ci-ar?
- Natrium (Na) har 1 valenselektron.
- Magnesium (Mg) har 2 valenselektroner.
- Aluminium (Al) har 3 valenselektroner.
- Silicium (Si) har 4 valenselektroner.
- Fosfor (P) har 5 valenselektroner.
- Svovl (S) har 6 valenselektroner.
- Klor (Cl) har 7 valenselektroner.
- Argon (Ar) har 8 valenselektroner.
Denne tendens er et resultat af det stigende atomnummer af grundstofferne. Når vi bevæger os fra venstre mod højre, øges antallet af protoner i kernen med én for hvert grundstof. Denne stigning i antallet af protoner tiltrækker flere elektroner til kernen, hvilket resulterer i en stigning i antallet af valenselektroner.
Antallet af valenselektroner er vigtigt, fordi det bestemmer et grundstofs kemiske egenskaber. Grundstoffer med det samme antal valenselektroner har en tendens til at have lignende kemiske egenskaber. For eksempel er natrium, kalium og cæsium alle alkalimetaller med 1 valenselektron. De reagerer alle på lignende måde med andre grundstoffer, såsom dannelse af +1 ioner.
Sidste artikelHvad er anvendelsen af jodtrichlorid?
Næste artikelKan du bruge hydrogenperoxid på piercinger?
 Varme artikler
Varme artikler
-
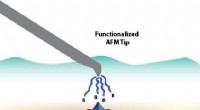 Virusoverflader hjælper ingeniører med at studere vaccine- og genterapiapplikationerEt isoelektrisk punkt er en almindelig måde at karakterisere vira på. Imidlertid, det er ikke nemt. For at forbedre fremstillingen af vacciner og genterapi, et Michigan Tech-team bruger overfladelad
Virusoverflader hjælper ingeniører med at studere vaccine- og genterapiapplikationerEt isoelektrisk punkt er en almindelig måde at karakterisere vira på. Imidlertid, det er ikke nemt. For at forbedre fremstillingen af vacciner og genterapi, et Michigan Tech-team bruger overfladelad -
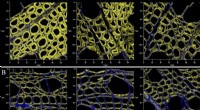 Kvantificering af ændringer i overfladekemi af træplanter under mikrobiel gæringORNL -forskere brugte sofistikerede laserscanningsteknikker til at sammenligne nedbrydningen af fermenteret populær (B) sammenlignet med ugæret populær (A), som de kvantificerede, for første gang, k
Kvantificering af ændringer i overfladekemi af træplanter under mikrobiel gæringORNL -forskere brugte sofistikerede laserscanningsteknikker til at sammenligne nedbrydningen af fermenteret populær (B) sammenlignet med ugæret populær (A), som de kvantificerede, for første gang, k -
 Metal organiske rammer metallisk beherskelseKredit:CC0 Public Domain De stramt definerede forhold mellem metaller i MOFer gør dem til ideelle udgangsmaterialer til skabelse af nye katalysatorer. Opvarmning af bimetalliske organiske metalst
Metal organiske rammer metallisk beherskelseKredit:CC0 Public Domain De stramt definerede forhold mellem metaller i MOFer gør dem til ideelle udgangsmaterialer til skabelse af nye katalysatorer. Opvarmning af bimetalliske organiske metalst -
 Forskerhold udvikler bioblæk til at printe terapeutiske midler i 3-DDr. Akhilesh K. Gaharwar, adjunkt ved Institut for Biomedicinsk Teknik, leder et forskningsprojekt for at udvikle en bioink-platform til sekvestrering af terapeutiske proteiner i en 3D-printet struktu
Forskerhold udvikler bioblæk til at printe terapeutiske midler i 3-DDr. Akhilesh K. Gaharwar, adjunkt ved Institut for Biomedicinsk Teknik, leder et forskningsprojekt for at udvikle en bioink-platform til sekvestrering af terapeutiske proteiner i en 3D-printet struktu
- Sådan beregnes Mass Flux
- Destination Moon:Er det tid for os at sende astronauter tilbage?
- Brandfordele
- Hvad er typer af tessellationer?
- Nyt aluminium og samarium hexaborid-baseret kompositmateriale med næsten nul ekspansion
- Troen på konspirationsteorier gør folk mere tilbøjelige til at engagere sig i kriminalitet på la…


