Hvilket atom har lignende egenskaber som oxygen?
Ilt og svovl er begge placeret i gruppe 16 (også kendt som chalcogenerne) i det periodiske system. Grundstoffer i samme gruppe deler lignende kemiske egenskaber på grund af tilstedeværelsen af det samme antal valenselektroner.
Både oxygen og svovl har seks valenselektroner og har tendens til at få to elektroner for at opnå en stabil elektronkonfiguration. Dette gør dem meget reaktive og danner kovalente bindinger med andre elementer for at fuldende deres ydre skal.
De deltager almindeligvis i kovalent binding for at fuldende deres ydre elektronskaller og demonstrere ikke-metalliske egenskaber. Ilt og svovl findes i forskellige allotropiske former, hvor oxygen har to stabile isotoper og svovl med fire stabile isotoper.
Ydermere viser oxygen og svovl en gradvis stigning i deres atomare og molekylære størrelser, når man bevæger sig ned i gruppen, hvilket resulterer i et fald i elektronegativitet og ioniseringsenergi.
 Varme artikler
Varme artikler
-
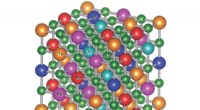 Uordnede materialer kan være hårdest, mest varmetolerante karbiderEn computermodel af atomstrukturen af et af de nye karbider. Det rodede rod af kulstof og fem metalelementer giver stabilitet til den overordnede struktur. Kredit:Pranab Sarker, Duke University
Uordnede materialer kan være hårdest, mest varmetolerante karbiderEn computermodel af atomstrukturen af et af de nye karbider. Det rodede rod af kulstof og fem metalelementer giver stabilitet til den overordnede struktur. Kredit:Pranab Sarker, Duke University -
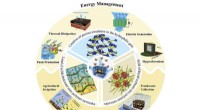 Hygroskopiske polymergeler:Opsamling af ferskvand og energi fra atmosfærisk fugtSyntesestrategier og AME-anvendelser af HPGer. Kredit:NIMTE Den globale befolkningseksplosion har udløst en enorm efterspørgsel efter ferskvand og energi. På trods af de store fremskridt inden for
Hygroskopiske polymergeler:Opsamling af ferskvand og energi fra atmosfærisk fugtSyntesestrategier og AME-anvendelser af HPGer. Kredit:NIMTE Den globale befolkningseksplosion har udløst en enorm efterspørgsel efter ferskvand og energi. På trods af de store fremskridt inden for -
 En nyopdaget katalysator lover billigere brintproduktionKredit:American Chemical Society En ny katalysator kan dramatisk reducere omkostningerne ved at producere brint, et af de reneste vedvarende brændstoffer. Baseret på molybdensulfid, katalysatoren
En nyopdaget katalysator lover billigere brintproduktionKredit:American Chemical Society En ny katalysator kan dramatisk reducere omkostningerne ved at producere brint, et af de reneste vedvarende brændstoffer. Baseret på molybdensulfid, katalysatoren -
 Hurtig test for at påvise salmonella i fødevarerTilfælde af salmonella-madforgiftning er et tilbagevendende fænomen. Råt kød er en hyppig smittekilde. Hvis rundstykket med svinetatar på billedet her var forurenet med patogener, at spise det kan før
Hurtig test for at påvise salmonella i fødevarerTilfælde af salmonella-madforgiftning er et tilbagevendende fænomen. Råt kød er en hyppig smittekilde. Hvis rundstykket med svinetatar på billedet her var forurenet med patogener, at spise det kan før
- Hybride glidende-rokkende brosøjler er mere jordskælvsbestandige
- Forskere afslører nyt princip for bevægelse i flydende krystaller
- Blå skraldespande flyder over med Amazon- og Walmart -kasser. Men var faktisk ved at genbruge mindr…
- Hvor meget tid mindre end månens tyngdekraft sammenlignet med jorden?
- En ballon vejer 1N er ophængt i luften og driver hverken op eller ned Hvor meget flydekraft virker …
- Undersøgte, hvorfor kvinder ikke er længere fremme i arbejdsstyrken end for 30 år siden


