Hvilket grundstof repræsenteret ved x reagerer med fluor for at danne forbindelsen XF2?
Fluor er det mest elektronegative element, hvilket betyder, at det har en stærk tendens til at tiltrække elektroner. Når fluor reagerer med et andet grundstof, danner det typisk en forbindelse, hvor fluor eksisterer som en anion (F-).
I forbindelsen XF2 skal grundstoffet x kunne miste to elektroner for at danne en kation (X2+), så det kan kombineres med to fluoranioner (2F-) og danne XF2.
I betragtning af grundstofferne i det periodiske system er det grundstof, der passer bedst til denne beskrivelse, calcium (Ca). Calcium tilhører gruppe 2, også kendt som jordalkalimetallerne, som er kendetegnet ved deres tendens til at miste to elektroner og danne 2+ kationer.
Når calcium reagerer med fluor, mister det to elektroner og danner calciumioner (Ca2+), som derefter kombineres med to fluoridioner (2F-) og danner calciumfluorid (CaF2).
Derfor er grundstoffet repræsenteret ved x calcium (Ca).
Sidste artikelHvordan finder man den molære masse af berylliumoxid?
Næste artikelHvad sker der, når der tilføres varme til et stof?
 Varme artikler
Varme artikler
-
 Lavpriskatalysator hjælper med at omdanne havvand til brændstof i stor skalaKredit:Pixabay/CC0 Public Domain Søværnets søgen efter at drive sine skibe ved at omdanne havvand til brændstof er et skridt nærmere. University of Rochester kemiingeniører, i samarbejde med fors
Lavpriskatalysator hjælper med at omdanne havvand til brændstof i stor skalaKredit:Pixabay/CC0 Public Domain Søværnets søgen efter at drive sine skibe ved at omdanne havvand til brændstof er et skridt nærmere. University of Rochester kemiingeniører, i samarbejde med fors -
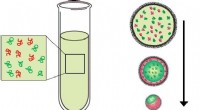 Cellestørrelse regulerer molekylær adskillelseVandig opløsning af to polymerer (rød og grøn) i et reagensglas og i kunstige celler af forskellig størrelse. I reagensglasset blandes opløsningen homogent, men i den lille kunstige celle skilles oplø
Cellestørrelse regulerer molekylær adskillelseVandig opløsning af to polymerer (rød og grøn) i et reagensglas og i kunstige celler af forskellig størrelse. I reagensglasset blandes opløsningen homogent, men i den lille kunstige celle skilles oplø -
 Nye fund om den største naturlige svovlkilde i atmosfærenLaboratorieopsætning af gratis jet-eksperimentet på TROPOS i Leipzig, som muliggør undersøgelse af den tidlige fase af oxidationsreaktioner under atmosfæriske forhold uden at væggene påvirker reaktion
Nye fund om den største naturlige svovlkilde i atmosfærenLaboratorieopsætning af gratis jet-eksperimentet på TROPOS i Leipzig, som muliggør undersøgelse af den tidlige fase af oxidationsreaktioner under atmosfæriske forhold uden at væggene påvirker reaktion -
 Ny teknik til at forbedre duktiliteten af keramiske materialer til missiler, motorerPurdue University-forskere har udviklet en ny proces for at hjælpe med at overvinde keramiks skøre natur og gøre den mere holdbar. Kredit:Purdue University/Chris Adam Noget så simpelt som et elekt
Ny teknik til at forbedre duktiliteten af keramiske materialer til missiler, motorerPurdue University-forskere har udviklet en ny proces for at hjælpe med at overvinde keramiks skøre natur og gøre den mere holdbar. Kredit:Purdue University/Chris Adam Noget så simpelt som et elekt
- Virgin Galactic gør satellit -lanceringstjeneste til et nyt selskab
- Kan atomkraft bekæmpe klimaændringer?
- Hvor meget vand løber der ind i landbrugsvanding?
- Bakterienedbrydende insektvinger inspirerer til ny antibakteriel emballage
- NASAs GPM viser nedbør sydøst for klippet Tropical Cyclone Iris
- Teknologi i klasseværelset kan forbedre primær matematik


