Hvilket fryser hurtigere ud af saltvandssukker og tryk på hvorfor?
Frysningspunktdepression
Det centrale koncept her er frysepunkt depression . Dette er fænomenet, hvor tilsætning af et opløsningsmiddel (som salt eller sukker) til et opløsningsmiddel (som vand) sænker frysepunktet for opløsningen sammenlignet med det rene opløsningsmiddel.
* saltvand: Salt (natriumchlorid) adskiller sig i ioner (Na+ og Cl-), når de opløstes i vand. Disse ioner forstyrrer dannelsen af den almindelige iskrystallstruktur, hvilket gør det sværere for vandet at fryse.
* sukkervand: Sukkermolekyler adskiller sig ikke i ioner, men de forstyrrer stadig vandmolekylernes evne til at danne den organiserede krystalstruktur, der er nødvendig til frysning.
* TAF VAND: Vand fra ledningsvandet indeholder typisk en lille mængde opløste mineraler, som muligvis kan sænke sit frysepunkt lidt sammenlignet med helt rent vand. Imidlertid er koncentrationen normalt for lav til at gøre en signifikant forskel i frysningstid.
Kortfattet:
* saltvand fryser den langsomste Fordi det har den største frysepunktdepression.
* sukkervand fryser langsommere end ledningsvand Fordi det også har et sænket frysepunkt.
* Tan Vand fryser den hurtigste Fordi det har den mindst mængde opløste stoffer, der påvirker dets frysepunkt.
Sidste artikelHvorfor smelter salt og sukker is?
Næste artikelHvilken russisk videnskabsmand relaterede kemiske egenskaber og atommasser?
 Varme artikler
Varme artikler
-
 Minimering af eksponering for skadelige flammehæmmende kemikalier i affaldsskum og plastKredit:Mary Ann Liebert, Inc., udgivere Fortsat forskning og nye politikker og praksis for at sikre korrekt brug og bortskaffelse af skum og plastprodukter, der indeholder potentielt skadelige fla
Minimering af eksponering for skadelige flammehæmmende kemikalier i affaldsskum og plastKredit:Mary Ann Liebert, Inc., udgivere Fortsat forskning og nye politikker og praksis for at sikre korrekt brug og bortskaffelse af skum og plastprodukter, der indeholder potentielt skadelige fla -
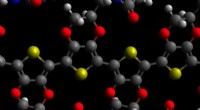 Cyborg-teknologi kunne muliggøre ny diagnostik, fusion af mennesker og AIMolekylær model af PEDOT med maleimid; kulstofatomer er grå, oxygen røde, nitrogen blå, svovler gule og hydrogener hvide. Kredit:David Martin Selvom sande cyborgs - delvist er menneskelige, delvis
Cyborg-teknologi kunne muliggøre ny diagnostik, fusion af mennesker og AIMolekylær model af PEDOT med maleimid; kulstofatomer er grå, oxygen røde, nitrogen blå, svovler gule og hydrogener hvide. Kredit:David Martin Selvom sande cyborgs - delvist er menneskelige, delvis -
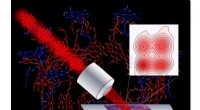 Forskere udvikler mikroskop til at spore lysenergistrøm i fotosyntetiske cellerAnvender en række ultrakorte laserpulser, et nyt mikroskop afslører indviklede detaljer, der styrer fotosyntetiske processer i lilla bakterier. Kredit:Vivek Tiwari, Yassel Acosta og Jennifer Ogilvie
Forskere udvikler mikroskop til at spore lysenergistrøm i fotosyntetiske cellerAnvender en række ultrakorte laserpulser, et nyt mikroskop afslører indviklede detaljer, der styrer fotosyntetiske processer i lilla bakterier. Kredit:Vivek Tiwari, Yassel Acosta og Jennifer Ogilvie -
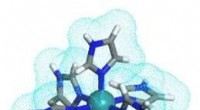 Nyt multi-protonbærerkompleks som en effektiv protonleder ved høje temperaturerForskere udvikler et meget symmetrisk ruthenium (III) kompleks med seks imidazol-imidazolatgrupper til effektiv højtemperaturprotonledning i brændselsceller. Kredit:Tokyo University of Science I ta
Nyt multi-protonbærerkompleks som en effektiv protonleder ved høje temperaturerForskere udvikler et meget symmetrisk ruthenium (III) kompleks med seks imidazol-imidazolatgrupper til effektiv højtemperaturprotonledning i brændselsceller. Kredit:Tokyo University of Science I ta
- Et urværk til venus
- Nedbrydning af Beowulf:Statistisk teknik finder bevis på, at gammelengelsk digt havde en enkelt for…
- Hvilken er den perfekte kvanteteori?
- Hvad er den samlede masse af protoner i et typisk ammoniak NH3 -molekyle?
- De 5 principper for Gestalt
- USA havde næsten rekordvarme, dyre vejrkatastrofer i 2016


