Hvorfor skal helium afkøles til 4K, før det kondenserer den grundlæggende proces?
1. Svage interatomiske kræfter:
* Heliumatomer er meget små og har en meget svag tiltrækning til hinanden. Dette skyldes deres elektronkonfiguration af lukket skal, hvilket gør dem meget stabile.
* Disse svage kræfter, kendt som Van der Waals -styrker, er ansvarlige for at holde molekyler sammen i væsker og faste stoffer.
2. Høj kinetisk energi:
* Ved stuetemperatur har heliumatomer en høj kinetisk energi. Dette betyder, at de bevæger sig meget hurtigt og kolliderer konstant med hinanden.
* De svage interatomiske kræfter er ikke stærke nok til at overvinde denne kinetiske energi og holde atomerne sammen i en flydende tilstand.
3. Kritisk temperatur og tryk:
* For at ethvert stof skal kondensere, skal det afkøles under dets kritiske temperatur. Ved denne temperatur er atomernes kinetiske energi lav nok til, at de svage interatomiske kræfter kan overvinde.
* Helium har en usædvanligt lav kritisk temperatur på 5,2k. Dette betyder, at det skal afkøles til næsten absolut nul (0 kelvin) for de svage interatomiske kræfter for at overvinde atomernes kinetiske energi.
4. Kondens ved 4K:
* Når helium afkøles under sin kritiske temperatur på 5,2K, begynder det at kondensere til en flydende tilstand.
* Ved 4K er heliumatomernes kinetiske energi lav nok til, at de svage interatomiske kræfter kan holde dem sammen i en væske.
* Yderligere afkøling til 2,17K omdanner flydende helium til en overfladisk, hvor det udviser forbløffende egenskaber som nul viskositet.
Kortfattet:
Heliums lave kritiske temperatur og svage interatomiske kræfter betyder, at det kræver ekstremt lave temperaturer for at overvinde den kinetiske energi fra sine atomer og kondensere til en væske. Denne unikke opførsel gør helium til en fremragende kryogen væske til applikationer som Superconductivity Research og MR -maskiner.
Sidste artikelKan du finde 26 videnskabelige termer?
Næste artikelHvilken type glas er den billigste sodavand Pyrex eller silica?
 Varme artikler
Varme artikler
-
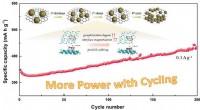 Partikelforfining inducerer og øger cykluskapaciteten af natrium/lithium-ion-batterierSkematisk diagram af mekanismen for partikelforfining for at inducere forøgelse af cykluskapaciteten af SIBer. Kredit:WANG Canpei Natriumionbatterier (SIBer) har tiltrukket bred opmærksomhed på
Partikelforfining inducerer og øger cykluskapaciteten af natrium/lithium-ion-batterierSkematisk diagram af mekanismen for partikelforfining for at inducere forøgelse af cykluskapaciteten af SIBer. Kredit:WANG Canpei Natriumionbatterier (SIBer) har tiltrukket bred opmærksomhed på -
 At møde en 100 år gammel udfordring kan føre vejen til digitale aromaerLugte kan måles ved deres afstand fra hinanden. Kredit:Weizmann Institute of Science Dufte – der lover mystik og intriger – blandes af mesterparfumører, deres opskrifter holdt hemmelige. I en ny u
At møde en 100 år gammel udfordring kan føre vejen til digitale aromaerLugte kan måles ved deres afstand fra hinanden. Kredit:Weizmann Institute of Science Dufte – der lover mystik og intriger – blandes af mesterparfumører, deres opskrifter holdt hemmelige. I en ny u -
 Højindeks overflade-eksponerede nanodendritter som ORR elektrokatalysatorVed hjælp af en atmosfære -skiftende strategi efterfulgt af elektrokemisk dealloying, forskere har syntetiseret sammensætningsgraderet PtCu 3 @Pt 3 Cu@Pt nanodendritter, der blotlægger overflader
Højindeks overflade-eksponerede nanodendritter som ORR elektrokatalysatorVed hjælp af en atmosfære -skiftende strategi efterfulgt af elektrokemisk dealloying, forskere har syntetiseret sammensætningsgraderet PtCu 3 @Pt 3 Cu@Pt nanodendritter, der blotlægger overflader -
 Forskere opfinder metode til at frigøre potentialet for meget brugt medicinKredit:CC0 Public Domain Sukkerarter som polysaccharider findes overalt i naturen og menes at være afgørende for, at der opstår liv. Hos mennesker, de dækker overfladen af alle celler og familie
Forskere opfinder metode til at frigøre potentialet for meget brugt medicinKredit:CC0 Public Domain Sukkerarter som polysaccharider findes overalt i naturen og menes at være afgørende for, at der opstår liv. Hos mennesker, de dækker overfladen af alle celler og familie
- Solceller til grønnere og sikrere energier
- Hvordan kan ozon være både godt og dårligt?
- Hvorfor nogle læger ønsker at defundere politiet
- Hvordan producerede victorianerne elektricitet?
- De globale emissioner er faldet med hidtil usete 7 % - men begynd ikke at fejre endnu
- Kaloriefattig diæt:Længere levetid?


