Hvordan produceres natriumsulfid?
1. Reaktion af natriumhydroxid (NaOH) med hydrogensulfid (H₂s):
Dette er den mest anvendte industrielle metode. Hydrogensulfidgas bobles gennem en opløsning af natriumhydroxid. Reaktionen producerer natriumsulfid og vand:
2NAOH (aq) + H₂s (g) → Na₂s (aq) + 2H₂O (l)
Denne reaktion udføres typisk ved forhøjede temperaturer for at forbedre reaktionshastigheden og effektiviteten.
2. Reduktion af natriumsulfat (na₂so₄) med kulstof:
Denne metode involverer opvarmning af natriumsulfat med kulstof i en ovn. Carbon reducerer sulfatet til sulfid og frigiver svovldioxid som et biprodukt:
na₂so₄ (s) + 4c (s) → NA₂s (s) + 4co (g)
Denne metode er mindre almindeligt anvendt end den første metode, men den er vigtig i nogle specifikke applikationer.
3. Direkte reaktion af natrium med svovl:
Denne metode er mindre praktisk til storstilet produktion på grund af sikkerhedsmæssige bekymringer og håndteringsvanskeligheder. Det demonstrerer dog den grundlæggende reaktion mellem elementerne:
2NA (S) + S (S) → NA₂S (S)
Andre metoder:
* Elektrolyse af natriumchlorid (NaCI) med svovldioxid (SO₂): Denne metode producerer natriumsulfid som et biprodukt af chlorproduktion.
* reaktion af natriumchlorid (NaCl) med svovl (r) og kulstof (C): Denne metode ligner reduktionen af natriumsulfat, men bruger natriumchlorid som udgangsmateriale.
Overvejelser:
* Produktionen af natriumsulfid resulterer typisk i en opløsning, der indeholder forskellige koncentrationer af natriumsulfid, vand og undertiden urenheder som natriumhydroxid.
* Afhængig af den tilsigtede anvendelse kan opløsningen koncentreres, oprenses eller behandles yderligere for at opnå fast natriumsulfid.
* Natriumsulfid er et meget reaktivt kemikalie og bør håndteres med forsigtighed.
Generelt involverer produktionen af natriumsulfid reaktion af natriumhydroxid med hydrogensulfid, skønt andre metoder også anvendes afhængigt af specifikke krav og tilgængelighed af råmaterialer.
 Varme artikler
Varme artikler
-
 En ny komposit til trækstyrkeStrand af menneskehår ved 200x forstørrelse. Kredit:Jan Homann/Wikipedia Materialeforskere er altid på udkig efter nye kompositter, materialer omfattende to eller flere forskellige stoffer, der ko
En ny komposit til trækstyrkeStrand af menneskehår ved 200x forstørrelse. Kredit:Jan Homann/Wikipedia Materialeforskere er altid på udkig efter nye kompositter, materialer omfattende to eller flere forskellige stoffer, der ko -
 Marengslignende materiale kunne gøre fly så støjsvage som en hårtørrerProfessor Michele Meo med letvægts aerogel ophængt i en honeycomb struktur. Kredit:University of Bath Et utroligt let nyt materiale, der kan reducere flymotorstøj og forbedre passagerkomforten, er
Marengslignende materiale kunne gøre fly så støjsvage som en hårtørrerProfessor Michele Meo med letvægts aerogel ophængt i en honeycomb struktur. Kredit:University of Bath Et utroligt let nyt materiale, der kan reducere flymotorstøj og forbedre passagerkomforten, er -
 Superhurtig metode til keramisk fremstilling kunne åbne døren til AI-drevet materialefundDigitale fotografier af UHS -sintringsprocessen for keramiske pellets. Kredit:Liangbing Hus gruppe ved University of Maryland, College Park Forskere ved University of Maryland (UMD) s Department o
Superhurtig metode til keramisk fremstilling kunne åbne døren til AI-drevet materialefundDigitale fotografier af UHS -sintringsprocessen for keramiske pellets. Kredit:Liangbing Hus gruppe ved University of Maryland, College Park Forskere ved University of Maryland (UMD) s Department o -
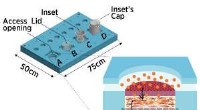 Rekonstruktion af hud på en chipMikrofluid hud-på-en-chip-enhed, der fungerer som et åbent system (A), en bioreaktor med låg (B), og et in vitro analysesystem udstyret med et åbent (C) eller et lukket skær (D). Nærbillede viser en g
Rekonstruktion af hud på en chipMikrofluid hud-på-en-chip-enhed, der fungerer som et åbent system (A), en bioreaktor med låg (B), og et in vitro analysesystem udstyret med et åbent (C) eller et lukket skær (D). Nærbillede viser en g
- Træd til side, indre tidevand:Supercomputermodellering forbedrer satellithøjdemålingspræcision
- Forskere undersøger årsager til ændring af landdækning i afrikanske savanner
- Video:Hvilken af disse svampe kan dræbe dig?
- Eng af dansende sprøde stjerner viser udviklingen på arbejde
- Trump udsætter beslutningen om klimaaftalen i Paris
- Hvad er rubidiumnitrat?


