Hvad er nogle måder, kromatografi kan adskille kemikalier i en blanding?
1. Adsorptionskromatografi:
* princip: Denne metode er afhængig af de forskellige affiniteter af komponenter til den stationære fase (normalt et fast adsorbent som silicagel eller aluminiumoxid). Komponenter, der binder stærkere til det stationære fase, bevæger sig langsommere gennem søjlen.
* Eksempler:
* Kolonnekromatografi: En lodret kolonne fyldt med den stationære fase. Blandingen påføres øverst, og den mobile fase (væske eller gas) strømmer igennem og adskiller komponenterne.
* Tyndlagskromatografi (TLC): Et tyndt lag adsorbent er belagt på en plade. Blandingen opdages i bunden, og den mobile fase bevæger sig op ad pladen ved kapillærvirkning og adskiller komponenterne.
2. Partitionskromatografi:
* princip: Denne metode udnytter de forskellige opløseligheder af komponenter i to ikke -blandbare faser (den stationære fase og den mobile fase). Komponenter, der er mere opløselige i den stationære fase, vil bevæge sig langsommere.
* Eksempler:
* gaskromatografi (GC): Den stationære fase er en ikke-flygtig væske, der er belagt på en solid støtte, og den mobile fase er en inert gas. Dette bruges til at adskille flygtige forbindelser.
* High-performance væskekromatografi (HPLC): Bruger en højtrykspumpe til at tvinge den mobile fase gennem en pakket søjle, der indeholder den stationære fase (normalt en væske). Dette er velegnet til at adskille en lang række forbindelser.
3. Ionbytningskromatografi:
* princip: Denne metode anvender ladede funktionelle grupper i den stationære fase til at binde ioner af modsat ladning fra blandingen. Forskellige ioner med forskellige affiniteter for den stationære fase er adskilt.
* Eksempler:
* kationbytterkromatografi: Bruger en negativt ladet stationær fase til at binde kationer.
* Anion Exchange Chromatography: Bruger en positivt ladet stationær fase til at binde anioner.
4. Størrelse-ekskluderingskromatografi (SEC):
* princip: Denne metode adskiller molekyler baseret på deres størrelse. Den stationære fase har porer i specifikke størrelser. Større molekyler kan ikke komme ind i porerne og passere hurtigere gennem søjlen, mens mindre molekyler kan komme ind i porerne og bevæge sig langsommere.
* Eksempler:
* gelfiltreringskromatografi: Bruger en gelmatrix som den stationære fase.
* gelpermeationskromatografi (GPC): Bruger en porøs polymer som den stationære fase.
5. Affinitetskromatografi:
* princip: Denne metode bruger en meget specifik interaktion mellem en komponent i blandingen og en ligand immobiliseret i den stationære fase. Dette giver mulighed for meget selektiv adskillelse.
* Eksempler:
* immunoaffinitetskromatografi: Bruger antistoffer som ligander til at binde og adskille specifikke proteiner.
* Metalaffinitetskromatografi: Bruger metalioner som ligander til at binde og separere proteiner med specifikke metalbindende steder.
Bemærk: Det specifikke valg af kromatografimetode afhænger af arten af blandingen, den ønskede adskillelse og egenskaberne ved forbindelserne. Hver metode har sine egne fordele og ulemper, og valget kræver ofte omhyggelig overvejelse.
Sidste artikelHvor er den metalliske karakter på periodisk tabel?
Næste artikelHvilken elektron kunne have kvantetal N4L2?
 Varme artikler
Varme artikler
-
 Almindelig ingrediens i husholdningsprodukter kan bidrage til antibiotikaresistensHolly Barrett, en ph.d.-kandidat i afdelingen for kemi, ledede en undersøgelse, der viste, at triclosan, der findes i mange almindelige husholdningsprodukter, er det fremherskende antibiotikum i Ontar
Almindelig ingrediens i husholdningsprodukter kan bidrage til antibiotikaresistensHolly Barrett, en ph.d.-kandidat i afdelingen for kemi, ledede en undersøgelse, der viste, at triclosan, der findes i mange almindelige husholdningsprodukter, er det fremherskende antibiotikum i Ontar -
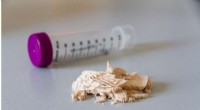 Bakterier fodret på en tilpasset diæt producerer biologisk nedbrydelige polymerer til alternativ e…Frysetørrede bakterier (Cupriavidus necator) før celleafbrydelse. Kredit:Fraunhofer-Gesellschaft Tyskland genererer omkring 38 kg plastaffald pr. indbygger hvert år. I et fælles projekt med Univer
Bakterier fodret på en tilpasset diæt producerer biologisk nedbrydelige polymerer til alternativ e…Frysetørrede bakterier (Cupriavidus necator) før celleafbrydelse. Kredit:Fraunhofer-Gesellschaft Tyskland genererer omkring 38 kg plastaffald pr. indbygger hvert år. I et fælles projekt med Univer -
 Ultrasensitiv giftig detektorEn skematisk illustration af gassensorenheden baseret på hybrid nanorod -arrays. Realtidsmodstanden versus tiden for det lodret justerede WO 3 -CuO core-shell nanorod-arrays-baseret gassensor til va
Ultrasensitiv giftig detektorEn skematisk illustration af gassensorenheden baseret på hybrid nanorod -arrays. Realtidsmodstanden versus tiden for det lodret justerede WO 3 -CuO core-shell nanorod-arrays-baseret gassensor til va -
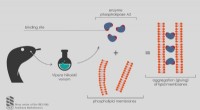 Kemikere opdagede, hvordan hugormegiften virkerKredit:Institut for Bioorganisk Kemi ved Det Russiske Videnskabsakademi Russiske videnskabsmænd rapporterer, at enzymet phospholipase A2 fra Vipera nikolskii-giften er i stand til at klæbe til lip
Kemikere opdagede, hvordan hugormegiften virkerKredit:Institut for Bioorganisk Kemi ved Det Russiske Videnskabsakademi Russiske videnskabsmænd rapporterer, at enzymet phospholipase A2 fra Vipera nikolskii-giften er i stand til at klæbe til lip
- Ny opdagelse komplicerer bestræbelserne på at måle universets ekspansion
- Den lyseste kosmiske eksplosion nogensinde:Hvordan vi kan have løst mysteriet, dets forvirrende ved…
- 300-års udtynding kan have disponeret Antarktis ishylder til at kollapse
- Forskere siger, at et skibsforlis ud for Patagonien er en forsvundet Rhode Island-hvalfanger fra 185…
- Hvad forsinkede Jordens iltning?
- Finde pulsen af den polære hvirvel


