Hvad er ligningen, der repræsenterer dissociation i opløsning af salt dannet ved en trivalent kation og bivalent anion?
Generel repræsentation
* kation: M 3+ (hvor m repræsenterer metallet)
* anion: X 2- (hvor X repræsenterer ikke-metalen)
Dissociation ligning
Den generelle ligning for dissociation af et sådant salt er:
M 2 X 3 (S) → 2m 3+ (aq) + 3x 2- (aq)
Forklaring
* m 2 X 3 (S): Dette repræsenterer det faste salt, før det opløses.
* →: Dette indikerer dissocieringsprocessen.
* 2m 3+ (aq): Dette viser de to trivalente kationer (m 3+ ) der frigøres i opløsningen, repræsenteret af (aq) for vandig.
* 3x 2- (aq): Dette viser de tre bivalente anioner (x 2- ) der frigøres i løsningen.
eksempel
Lad os tage eksemplet med aluminiumoxid (AL 2 O 3 ):
Al 2 O 3 (S) → 2Al 3+ (aq) + 3o 2- (aq)
Vigtige noter:
* Underskrifterne i den kemiske formel (f.eks. 2 og 3 i Al 2 O 3 ) Angiv forholdet mellem kationer og anioner i saltet.
* Koefficienterne i den afbalancerede ligning (f.eks. 2 og 3 i dissocieringsligningen) repræsenterer antallet af ioner, der er frigivet pr. Formelenhed for saltet.
* Dette er en forenklet repræsentation. Den faktiske dissocieringsproces kan involvere hydrering af ioner med vandmolekyler i opløsningen.
Sidste artikelHvad er et synonym for et atomnummer?
Næste artikelHvornår fandt den første nukleosyntese sted?
 Varme artikler
Varme artikler
-
 Forskere løser det 100-årige metallurgipuslespilFor at forstå præcis, hvordan metaller reagerer på højhastighedskomprimering i molekylære dynamiksimuleringer, LLNL -forskere bruger nye metoder til silikomikroskopi til at afsløre defekter i krystalg
Forskere løser det 100-årige metallurgipuslespilFor at forstå præcis, hvordan metaller reagerer på højhastighedskomprimering i molekylære dynamiksimuleringer, LLNL -forskere bruger nye metoder til silikomikroskopi til at afsløre defekter i krystalg -
 Portrætter af partiklerKredit:Duke University På solparker på særligt støvede steder i verden, ligesom den arabiske halvø og dele af Indien og Kina, luftforurening koster solenergiindustrien titusinder af milliarder af
Portrætter af partiklerKredit:Duke University På solparker på særligt støvede steder i verden, ligesom den arabiske halvø og dele af Indien og Kina, luftforurening koster solenergiindustrien titusinder af milliarder af -
 Undersøgelse viser, hvordan små rum kunne have været forud for cellerForskere brugte Argonnes Advanced Photon Source til at studere membranløse rum kaldet komplekse coacervater, da de gennemgik våd-tør-cykler, en undersøgelse, der kaster lys over den prebiotiske jord o
Undersøgelse viser, hvordan små rum kunne have været forud for cellerForskere brugte Argonnes Advanced Photon Source til at studere membranløse rum kaldet komplekse coacervater, da de gennemgik våd-tør-cykler, en undersøgelse, der kaster lys over den prebiotiske jord o -
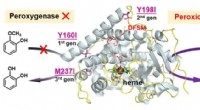 Konvertering af P450 peroxygenase til peroxidase via mekanismestyret proteinteknologiFunktionel omdannelse af peroxygenase til peroxidase i DFSM-faciliteret P450BM3-H 2 O 2 system. Kredit:Ma Nana Enzymkatalyse er en lovende grøn løsning til fremstilling af lægemidler, fine kem
Konvertering af P450 peroxygenase til peroxidase via mekanismestyret proteinteknologiFunktionel omdannelse af peroxygenase til peroxidase i DFSM-faciliteret P450BM3-H 2 O 2 system. Kredit:Ma Nana Enzymkatalyse er en lovende grøn løsning til fremstilling af lægemidler, fine kem
- Sådan fungerer svævefly
- Hvad er den nemmeste måde at konvertere centimeter inches på?
- Forudsige, hvordan klimaændringer vil påvirke distributionen af tropiske fisk i Japan
- Afstemning viser, at sociale netværk er stærke som reaktion på COVID-19-krisen
- Schumer foreslår 462 milliarder dollars bilbytte - gas til el
- Trykt polymer giver forskere mulighed for at udforske chiralitet og spin-interaktioner ved stuetempe…


