Ville du forvente, at iod vil fortrænge brom fra en opløsning af kaliumbromid?
* reaktivitetsserie: Jod er mindre reaktiv end brom. Dette betyder, at jod er mere tilbøjelig til at miste elektroner og blive en ion (I-) sammenlignet med brom.
* forskydningsreaktion: I en forskydningsreaktion fortrænger et mere reaktivt element et mindre reaktivt element fra dets forbindelse.
* reaktionen: Når jod tilsættes til en opløsning af kaliumbromid, opstår følgende reaktion:
`` `
I2 (s) + 2kbr (aq) → 2ki (aq) + br2 (l)
`` `
* observationer: Du vil observere dannelsen af en brun/rødlig væske, som er elementær brom (BR2) og en farveløs opløsning af kaliumiodid (KI).
Kortfattet: Jod er mere reaktiv end brom, så det kan fortrænge brom fra en opløsning af kaliumbromid. Dette er et klassisk eksempel på en forskydningsreaktion.
 Varme artikler
Varme artikler
-
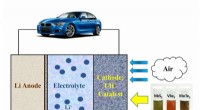 2-D-materialer kan gøre det muligt for elektriske køretøjer at komme 500 miles på en enkelt opla…2D-katalysatorer driver et elektrisk køretøj. Kredit:Amin Salehi-Khojin Lithium-luft-batterier er klar til at blive den næste revolutionerende erstatning for aktuelt brugte lithium-ion-batterier,
2-D-materialer kan gøre det muligt for elektriske køretøjer at komme 500 miles på en enkelt opla…2D-katalysatorer driver et elektrisk køretøj. Kredit:Amin Salehi-Khojin Lithium-luft-batterier er klar til at blive den næste revolutionerende erstatning for aktuelt brugte lithium-ion-batterier, -
 Forskere udvikler dynamiske skabeloner, der er afgørende for printbar elektronikteknologiFra nederst til højre, med uret:Ying Diao og Diwakar Shukla, professorer i kemisk og biomolekylær teknik; Chuankai Zhao og Erfan Mohammadi, kandidatstuderende. Kredit:L. Brian Stauffer Når det kom
Forskere udvikler dynamiske skabeloner, der er afgørende for printbar elektronikteknologiFra nederst til højre, med uret:Ying Diao og Diwakar Shukla, professorer i kemisk og biomolekylær teknik; Chuankai Zhao og Erfan Mohammadi, kandidatstuderende. Kredit:L. Brian Stauffer Når det kom -
 Lægemiddel mod superbakterier fundet i kråbærEt urinkateter belagt med antimikrobielle peptider forhindrer alvorlige urinvejsinfektioner. Docent Anna Maria Pirttilä og CEO Mysore Tejesvi fra Chain Antimicrobials Oy er personerne bag peptidinnova
Lægemiddel mod superbakterier fundet i kråbærEt urinkateter belagt med antimikrobielle peptider forhindrer alvorlige urinvejsinfektioner. Docent Anna Maria Pirttilä og CEO Mysore Tejesvi fra Chain Antimicrobials Oy er personerne bag peptidinnova -
 Forskere afslører strukturen af aminosyretransportør involveret i kræftForskere fra University of Groningen involveret i undersøgelsen - venstre til højre, stående:D.J. Slotboom, A. Guskov, A.A. Garaeva, C. Paulino - siddende:G.T. Oostergetel. Kredit:University of Gronin
Forskere afslører strukturen af aminosyretransportør involveret i kræftForskere fra University of Groningen involveret i undersøgelsen - venstre til højre, stående:D.J. Slotboom, A. Guskov, A.A. Garaeva, C. Paulino - siddende:G.T. Oostergetel. Kredit:University of Gronin
- Hvad er det vigtigste kendetegn ved en svampe?
- Cinema -abonnementstjeneste MoviePass lukker ned
- Ikke alle sorte landskaber er dårlige. Vi skal lære at elske den rigtige slags
- La Nina-lignende havafkølingsmønstre intensiverer tropiske cykloner i det nordvestlige Stillehav
- Hvordan ændrer folk en vulkan?
- Forskere foreslår redox-mekanisme til vand-gas-skiftreaktion


