Hvad tegner sig for metalens egenskaber?
1. Metallisk binding:
* Hav af elektroner: Metalatomer har løst bundne valenselektroner, der let løsnes fra deres overordnede atomer. Disse elektroner danner et "hav" af delokaliserede elektroner, der er frie til at bevæge sig gennem hele metalgitteret.
* Elektrostatisk attraktion: De positivt ladede metalioner holdes sammen af den stærke elektrostatiske tiltrækning til det omgivende hav af elektroner. Denne limning er ikke-retningsbestemt, hvilket muliggør fleksibilitet og formbarhed.
2. Atomstruktur:
* Luk pakning: Metalatomer har en tendens til at have relativt store atomradier og et enkelt, regelmæssigt arrangement i deres krystalgitter. Denne tæt pakning maksimerer samspillet mellem atomer og bidrager til deres høje densitet.
* krystalstruktur: Metaller krystalliserer ofte i tætpakkede strukturer som ansigtscentreret kubisk (FCC) eller kropscentreret kubik (BCC), der giver stabilitet og styrke.
3. Egenskaber og deres forhold til struktur:
* Konduktivitet (elektrisk og termisk): De frit bevægende elektroner i den metalliske binding giver mulighed for let overførsel af elektrisk ladning og termisk energi, hvilket gør metaller fremragende ledere.
* formbarhed og duktilitet: Den ikke-retningsbestemte binding og tætpakket struktur tillader metalatomer at glide forbi hinanden uden at bryde bindinger. Dette gør det muligt for metaller at blive hamret i ark (formbarhed) eller tegnet i ledninger (duktilitet).
* Luster: De frie elektroner i metaller kan let absorbere og genemitere lys, hvilket giver dem et skinnende udseende (glans).
* styrke og hårdhed: Selvom det ikke altid er de sværeste materialer, kan metaller være meget stærke på grund af den stærke metalliske binding og tæt pakning af atomer.
* smelte- og kogepunkter: Den stærke metalliske binding kræver betydelig energi til at bryde, hvilket resulterer i høje smelte- og kogepunkter for de fleste metaller.
Kortfattet: Kombinationen af metallisk binding med en specifik atomstruktur tegner sig for metallers karakteristiske egenskaber. Disse egenskaber gør metaller meget nyttige i en lang række applikationer, fra byggematerialer og elektriske ledninger til smykker og maskiner.
Sidste artikelHvordan leveres naturgas?
Næste artikelVille du forvente, at iod vil fortrænge brom fra en opløsning af kaliumbromid?
 Varme artikler
Varme artikler
-
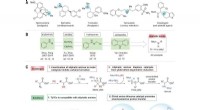 Brug af en to-trins tilgang til at omdanne alifatiske aminer til unaturlige aminosyrerStrategi for enantiokontrol af N-H insertionsreaktioner af alifatiske aminer med carbener. (A) Repræsentative lægemidler, der demonstrerer allestedsnærværelsen af chirale alifatiske aminer i bioakti
Brug af en to-trins tilgang til at omdanne alifatiske aminer til unaturlige aminosyrerStrategi for enantiokontrol af N-H insertionsreaktioner af alifatiske aminer med carbener. (A) Repræsentative lægemidler, der demonstrerer allestedsnærværelsen af chirale alifatiske aminer i bioakti -
 Forskere forsøger at printe tyndfilmstransistorer med metaloxider på varmefølsomme materialerFleksibel:Elektroniske kredsløb på en film af polyimid fra Empa-laboratoriet danner synaptiske transistorer. Kredit:Empa Inden for projektet Functional Oxides Printed on Polymers and Paper (FOXIP)
Forskere forsøger at printe tyndfilmstransistorer med metaloxider på varmefølsomme materialerFleksibel:Elektroniske kredsløb på en film af polyimid fra Empa-laboratoriet danner synaptiske transistorer. Kredit:Empa Inden for projektet Functional Oxides Printed on Polymers and Paper (FOXIP) -
 Tredobling af effektiviteten af solbaseret brintbrændstofproduktion med metalliske nanostrukturer…Et nanostruktureret metamateriale med et solsikke-lignende arrangement kan nedsænkes i vand for at generere hydrogengas med en suveræn effektivitet. Kredit:WILEY-VCH Verlag GmbH &Co. Hydrogengas,
Tredobling af effektiviteten af solbaseret brintbrændstofproduktion med metalliske nanostrukturer…Et nanostruktureret metamateriale med et solsikke-lignende arrangement kan nedsænkes i vand for at generere hydrogengas med en suveræn effektivitet. Kredit:WILEY-VCH Verlag GmbH &Co. Hydrogengas, -
 Forskere udvikler en bærbar enhed, der skaber 3D-billeder af huden på 10 minutterMr Fu Xiaoxu holder den bærbare hudkortlægningsenhed op, som kun vejer 100 gram og er på størrelse med et kreditkort. Kredit:Nanyang Technological University Et team fra Nanyang Technological Univ
Forskere udvikler en bærbar enhed, der skaber 3D-billeder af huden på 10 minutterMr Fu Xiaoxu holder den bærbare hudkortlægningsenhed op, som kun vejer 100 gram og er på størrelse med et kreditkort. Kredit:Nanyang Technological University Et team fra Nanyang Technological Univ
- Højere opløsning i havmodeller:Er det det værd?
- Hvilken matematik klasse over beregningen har brug for mekaniske ingeniører?
- Påvirker lav temperatur funktionen af en celle?
- Hvem observerer observatørerne? Forskere udfører storstilet undersøgelse af iNaturalist-brugere
- Når den fremadrettede inerti af et projektil afbalancerer nedadgående træk tyngdekraften er?
- Hvorfor bliver månen i sin bane og flyver ikke ud i rummet?


