Hvilket udstyr bruges i laboratoriet til at bestemme specifik varme af et stof?
Væsentligt udstyr:
1. kalorimeter: Dette er hjertet af eksperimentet. En kalorimeter er en enhed designet til at måle varmestrømmen ind eller ud af et system. Der er to hovedtyper:
* Enkel kalorimeter: Ofte en Styrofoam -kop eller en simpel isoleret beholder, der hjælper med at minimere varmetab til omgivelserne.
* bombe kalorimeter: Et mere sofistikeret instrument, der ofte bruges til forbrændingsreaktioner. Det har et forseglet kammer, hvor stoffet brændes, og dets temperaturændring måles omhyggeligt.
2. Varmeindretning: Du har brug for en kontrolleret måde at varme stoffet på. Dette kan være:
* Bunsen Burner: En almindelig gasdrevet brænder til opvarmning.
* hot plade: En elektrisk opvarmningsoverflade til mere kontrolleret temperatur.
* Vandbad: En beholder med vand opvarmet til en bestemt temperatur.
3. termometer: Afgørende for at måle temperaturændringen af både stoffet og vandet i kalorimeteret. Digitale termometre foretrækkes ofte for nøjagtighed.
4. skala eller balance: Behov for nøjagtigt at måle stoffets masse og alt anvendt vand.
5. bægerglas eller kolbe: Containere til at holde stoffet, vandet og for at give mulighed for sikker blanding.
6. omrørestang eller omrører: For at sikre jævn varmefordeling og blanding.
Yderligere udstyr (valgfrit):
* omrøringsmotor: For mere kontrolleret og konsekvent omrøring.
* datalogger: At automatisk registrere temperaturaflæsninger over tid for mere detaljeret analyse.
* computer: At analysere dataene og beregne den specifikke varme.
Nøglekoncepter:
* Specifik varme: Mængden af varmeenergi, der kræves for at hæve temperaturen på et gram af et stof med en grad Celsius (eller Kelvin).
* kalorimetri: Processen med at måle varmestrømmen ind eller ud af et system.
* Varmeoverførsel: Bevægelsen af varmeenergi fra et objekt eller et system til et andet.
procedure (forenklet):
1. måle stoffets masse.
2. Mål den oprindelige temperatur på stoffet.
3.
4. Overfør det opvarmede stof til kalorimeteret indeholdende en kendt masse vand ved en kendt temperatur.
5. Mål den endelige temperatur på vand- og stofblandingen.
6. Beregn den varme, der er opnået ved vandet ved hjælp af formlen:
Q =m * c * ΔT
(Hvor q er varme, m er masse, c er specifik varme, og ΔT er temperaturændringen)
7. Beregn den varme, der er mistet af stoffet.
8. Brug de beregnede varmeværdier og stoffets masse til at bestemme dets specifikke varme.
Fortæl mig, hvis du vil have en mere detaljeret forklaring af de specifikke trin, der er involveret i et bestemt eksperiment.
Sidste artikelHvor mange elektronprikker skal arsen have?
Næste artikelKan ilt opsamles ved nedadgående forskydning af vand?
 Varme artikler
Varme artikler
-
 Forskningslaboratoriesimulator fuldfører væsentligt lægemiddelopdagelsesarbejde på få dageJohn Wise. Kredit:Southern Methodist University, Hillsman S. Jackson SMU-forskere har udviklet et sæt computerdrevne rutiner, der kan efterligne kemiske reaktioner i et laboratorium, at reducere d
Forskningslaboratoriesimulator fuldfører væsentligt lægemiddelopdagelsesarbejde på få dageJohn Wise. Kredit:Southern Methodist University, Hillsman S. Jackson SMU-forskere har udviklet et sæt computerdrevne rutiner, der kan efterligne kemiske reaktioner i et laboratorium, at reducere d -
 Beskyttelse af natriummetalanoder møder in situ fotoelektronspektroskopiSpecialdesignet flerkammersystem med karakteriseringer af ultraviolet fotoelektronspektroskopi (UPS) og røntgenfotoelektronspektroskopi (XPS). Nøgleresultater af dette arbejde. Kredit:Yuan Liu, Xu Lia
Beskyttelse af natriummetalanoder møder in situ fotoelektronspektroskopiSpecialdesignet flerkammersystem med karakteriseringer af ultraviolet fotoelektronspektroskopi (UPS) og røntgenfotoelektronspektroskopi (XPS). Nøgleresultater af dette arbejde. Kredit:Yuan Liu, Xu Lia -
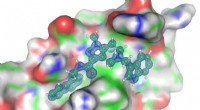 Ny terapeutisk strategi mod sovesygeStruktur af grænsefladen mellem PEX14 og PEX5 (bagpå) inklusive strukturen af inhibitoren (foran). Kredit:Dr. Grzegorz Popowicz, Helmholtz Zentrum München Et nyudviklet lille molekyle dræber sel
Ny terapeutisk strategi mod sovesygeStruktur af grænsefladen mellem PEX14 og PEX5 (bagpå) inklusive strukturen af inhibitoren (foran). Kredit:Dr. Grzegorz Popowicz, Helmholtz Zentrum München Et nyudviklet lille molekyle dræber sel -
 Opdeling af vandmolekyler til en fremtid med vedvarende energiKemi kandidatstuderende Zhijie Yang driver synkrotronmålecomputer på Advanced Photon Source i Argonne National Lab på et foto taget før COVID-19-pandemien. Kredit:Virginia Tech Den fremtidige økon
Opdeling af vandmolekyler til en fremtid med vedvarende energiKemi kandidatstuderende Zhijie Yang driver synkrotronmålecomputer på Advanced Photon Source i Argonne National Lab på et foto taget før COVID-19-pandemien. Kredit:Virginia Tech Den fremtidige økon
- Hvilken planet har en giftig atmosfære, end der er så tyk og sur, selv sonder har problemer med at…
- Jordnødder, der gør mere med mindre vand
- Hvilken del af DNA giver koden til proteiner?
- Udtørret Mendocino, Californien, opfordrer gæsterne til at spare på vandet
- Kraftig tyfon rammer Filippinerne, forkæler julen (opdatering)
- Hvor stor er jorden i centimeter?


