Hvordan er gasserne af?
* Ingen fast form eller volumen: Gasser tager form og volumen på deres beholder.
* Kompressibilitet: Gasser kan komprimeres, hvilket betyder, at deres volumen kan reduceres ved at anvende tryk.
* udvidelighed: Gasser udvides for at udfylde hele den tilgængelige plads.
* lav densitet: Gasser er generelt meget mindre tætte end faste stoffer eller væsker.
* høj kinetisk energi: Gasmolekyler har høj kinetisk energi og bevæger sig hurtigt i tilfældige retninger.
* svage intermolekylære kræfter: De attraktive kræfter mellem gasmolekyler er svage, så de kan bevæge sig frit.
* diffusion: Gasser kan diffundere til hinanden, hvilket betyder, at de blander spontant.
Eksempler på gasser:
* Ilt (O2)
* Nitrogen (N2)
* Kuldioxid (CO2)
* Helium (han)
* Methan (CH4)
Fortæl mig, hvis du har andre spørgsmål eller gerne vil vide mere om specifikke gasser!
Sidste artikelHvornår bliver vand en gas?
Næste artikelHvad er de kemiske reaktioner i forbrændingsmotoren?
 Varme artikler
Varme artikler
-
 At opnå stærke strukturer med kulfiberforstærket plastEn fejl på grund af den klassiske globale knækning af søjlen med begge endestifter opleves af den ustyrkede kontrolprøve, (en). Sammenlignet med formen af kontrolprøverne, den deformerede form af al
At opnå stærke strukturer med kulfiberforstærket plastEn fejl på grund af den klassiske globale knækning af søjlen med begge endestifter opleves af den ustyrkede kontrolprøve, (en). Sammenlignet med formen af kontrolprøverne, den deformerede form af al -
 Oxidsintring ved lufttrykskontrolOpstilling af en prøve i en lufttryksreguleringsatmosfæreovn. Kredit:Toyohashi University of Technology Professor Hiromi Nakano fra Toyohashi University of Technology har samarbejdet med en virkso
Oxidsintring ved lufttrykskontrolOpstilling af en prøve i en lufttryksreguleringsatmosfæreovn. Kredit:Toyohashi University of Technology Professor Hiromi Nakano fra Toyohashi University of Technology har samarbejdet med en virkso -
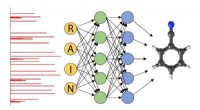 Den næste fase:Brug af neurale netværk til at identificere gasfasemolekylerDette skema over et neuralt netværk viser tildelingen af rotationsspektre (røde bjælker til venstre) af en algoritme (midten) til at identificere strukturen af et molekyle i gasfasen (højre). Kred
Den næste fase:Brug af neurale netværk til at identificere gasfasemolekylerDette skema over et neuralt netværk viser tildelingen af rotationsspektre (røde bjælker til venstre) af en algoritme (midten) til at identificere strukturen af et molekyle i gasfasen (højre). Kred -
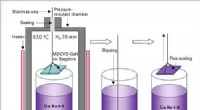 Udvikling af en ny teknik til dyrkning af højkvalitets galliumnitridkrystallerFigur 1. Skematisk af GaN-krystalvækstteknikken ved anvendelse af Flux-Film-Coated Liquid Phase Epitaxy (FFC-LPE) teknikken. Kredit:National Institute for Materials Science Galliumnitridkrystaller
Udvikling af en ny teknik til dyrkning af højkvalitets galliumnitridkrystallerFigur 1. Skematisk af GaN-krystalvækstteknikken ved anvendelse af Flux-Film-Coated Liquid Phase Epitaxy (FFC-LPE) teknikken. Kredit:National Institute for Materials Science Galliumnitridkrystaller
- Konverter 112 grader Fahrenheit til celsius?
- Hvad tænker du på? Facebook siger, at nøgne statuer ikke burde være det
- Tricks til at huske de polyatomiske ion
- Test af Vlad the Impalers breve viser, at han kan have haft en tilstand, der forårsagede, at hans t…
- Udløste en nikkel hungersnød den 'store oxidationsbegivenhed'?
- Kunne mørke baryoner forklare stof?


