Hvor mange mol H2O er produkt fra reaktion 355 G O2?
1. Skriv den afbalancerede kemiske ligning:
2 H₂ + O₂ → 2 H₂O
2. Konverter gram O₂ til mol:
* Molmasse O₂ =32 g/mol
* Mol O₂ =(355 g o₂) / (32 g / mol) =11,09 mol o₂
3. Brug molforholdet fra den afbalancerede ligning:
* Den afbalancerede ligning viser, at 1 mol O₂ producerer 2 mol H₂O.
4. Beregn mol H₂O:
* Mol H₂O =(11,09 mol O₂) * (2 mol H₂O / 1 mol O₂) = 22,18 mol H₂O
Derfor vil 355 g O₂ producere 22,18 mol H₂O.
Sidste artikelHar ethvert stof tredobbelt punkt?
Næste artikelHvorfor er deicer salt virkelig godt at smelte sne?
 Varme artikler
Varme artikler
-
 Bakteriefælde kan hjælpe med at bremse antibiotikaresistensKredit:CC0 Public Domain Forskere har udviklet en ny og hurtigere test til at identificere, hvordan enkelte bakterier reagerer på antibiotika, som kunne hjælpe i kampen mod antimikrobiel resistens
Bakteriefælde kan hjælpe med at bremse antibiotikaresistensKredit:CC0 Public Domain Forskere har udviklet en ny og hurtigere test til at identificere, hvordan enkelte bakterier reagerer på antibiotika, som kunne hjælpe i kampen mod antimikrobiel resistens -
 Dehydrerer planteproteiner med lydens hastighedEfter 8 minutter, den tørrede gel danner flager, der er lette og ikke-klæbende. Foto af Fred Zwicky Næsten alle kender til ultralyd – de højfrekvente lydbølger, der hopper rundt i kroppen og skabe
Dehydrerer planteproteiner med lydens hastighedEfter 8 minutter, den tørrede gel danner flager, der er lette og ikke-klæbende. Foto af Fred Zwicky Næsten alle kender til ultralyd – de højfrekvente lydbølger, der hopper rundt i kroppen og skabe -
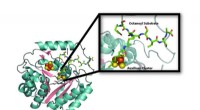 Vedvarende ressource:For at producere vital liponsyre, svovl bruges, derefter genopfyldesModel af krystalstrukturen af lipoylsyntaseenzymet (LipA) fra bakterierne Mycobacterium tuberculosis, der afslører ødelæggelsen af en af dens jern-svovlklynger (orange og gule kugler) til brug s
Vedvarende ressource:For at producere vital liponsyre, svovl bruges, derefter genopfyldesModel af krystalstrukturen af lipoylsyntaseenzymet (LipA) fra bakterierne Mycobacterium tuberculosis, der afslører ødelæggelsen af en af dens jern-svovlklynger (orange og gule kugler) til brug s -
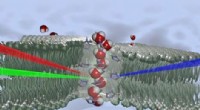 Kunstige bio-inspirerede membraner til vandfiltreringSkematisk repræsentation af vandmolekyler med en trådlignende struktur orienteret i en enkelt retning i kernen af en kanal, vist som gennemsigtig. Dannet af histaminderivater, denne chirale kanal da
Kunstige bio-inspirerede membraner til vandfiltreringSkematisk repræsentation af vandmolekyler med en trådlignende struktur orienteret i en enkelt retning i kernen af en kanal, vist som gennemsigtig. Dannet af histaminderivater, denne chirale kanal da
- Atmosfæriske forskere studerer brande for at løse isspørgsmål i klimamodeller
- Hawaii -teleskopprotester får tilhængere til at forsvare projektet
- Hvordan udryddelsen af istidens pattedyr kan have tvunget mennesker til at opfinde civilisationen
- Er transportprotein påkrævet til ikke -polære molekyler?
- Hvilken planet kaldes Messenger af romerske guder?
- Ny elektrokemisk biosensor til tidlig kræftpåvisning


