Er et atom, der har det samme antal protoner som neutroner et neutralt atom?
* Protoner bestemmer elementet: Antallet af protoner definerer, hvad element et atom er. For eksempel har alle carbonatomer 6 protoner.
* neutroner påvirker isotopen: Antallet af neutroner bestemmer isotopen af et element. For eksempel har carbon-12 6 neutroner, mens carbon-14 har 8 neutroner.
* Elektroner bestemmer ladning: Et atom er neutral, når det har et lige antal protoner (positiv ladning) og elektroner (negativ ladning). Antallet af neutroner påvirker ikke direkte ladningen.
Eksempel:
* Et carbon-12-atom har 6 protoner, 6 neutroner og 6 elektroner. Dette atom er neutral.
* Et carbon-14-atom har også 6 protoner, men det har 8 neutroner. For at forblive neutral har det stadig brug for 6 elektroner.
Konklusion: Mens antallet af protoner og neutroner er vigtige for at definere en atoms identitet, er det antallet af elektroner, der dikterer, om et atom er neutralt eller har en ladning.
 Varme artikler
Varme artikler
-
 Brændselscelle fremme et frisk pust til fremtidigt kraftalternativFast oxid brændselsceller kan bruges i en række forskellige applikationer, herunder effektiv generering af primær- eller nødstrømforsyning til bygninger. En gruppe Bloom Energy-servere genererer strøm
Brændselscelle fremme et frisk pust til fremtidigt kraftalternativFast oxid brændselsceller kan bruges i en række forskellige applikationer, herunder effektiv generering af primær- eller nødstrømforsyning til bygninger. En gruppe Bloom Energy-servere genererer strøm -
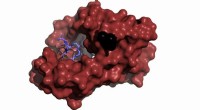 Mutationer i nøgleprotein, der overvåger cellulære funktioner, der er afgørende for sundhed og o…En overfladerepræsentation af sygdomsmutanten CaM (D95V, rød) i kompleks med stykket af den spændingsregulerede calciumkanal (blå). Kredit:Canadian Light Source Et nyt forskningsprojekt bruger den
Mutationer i nøgleprotein, der overvåger cellulære funktioner, der er afgørende for sundhed og o…En overfladerepræsentation af sygdomsmutanten CaM (D95V, rød) i kompleks med stykket af den spændingsregulerede calciumkanal (blå). Kredit:Canadian Light Source Et nyt forskningsprojekt bruger den -
 Kan jeg blande disse kemikalier? Der er en app til det!En visuel fremstilling, der viser, hvordan tildeling af graffarveregistre fungerer. Kredit:Jason Ott/UCR Forkert blandede kemikalier forårsager et chokerende antal brande, eksplosioner, og skader
Kan jeg blande disse kemikalier? Der er en app til det!En visuel fremstilling, der viser, hvordan tildeling af graffarveregistre fungerer. Kredit:Jason Ott/UCR Forkert blandede kemikalier forårsager et chokerende antal brande, eksplosioner, og skader -
 DNA er kun et blandt millioner af mulige genetiske molekylerKredit:CC0 Public Domain Biologi koder information i DNA og RNA, som er komplekse molekyler finjusteret til deres funktioner. Men er de den eneste måde at gemme arvelig molekylær information? Nogl
DNA er kun et blandt millioner af mulige genetiske molekylerKredit:CC0 Public Domain Biologi koder information i DNA og RNA, som er komplekse molekyler finjusteret til deres funktioner. Men er de den eneste måde at gemme arvelig molekylær information? Nogl
- Hvorfor golfbanegræs ser så perfekt ud
- Hvorfor er farve vigtig i naturen?
- Anmeldelse:2023 Toyota bZ4X vs. 2023 Volkswagen ID.4
- Twitters grænse på 140 tegn - tid til at droppe det?
- Fremskridt inden for risgenomforskning giver indsigt og lovende anvendelser for landbruget
- Hvorfor er cellemembranen og væggen nødvendig?


