Hvad kaldes kemisk reaktion med brint?
Typer af reaktioner:
* Hydrogenering: Dette er det mest almindelige udtryk, og det beskriver tilsætningen af brint til et molekyle, normalt en umættet organisk forbindelse. Dette katalyseres ofte af en metalkatalysator.
* reduktion: I mange tilfælde fungerer brint som et reduktionsmiddel, hvilket betyder, at det donerer elektroner til et andet stof. Dette er et bredt udtryk, der omfatter mange typer reaktioner.
* forbrænding: Når brint reagerer med ilt, brænder det for at producere vand og varme. Dette er en meget eksoterm reaktion.
* syre-base-reaktioner: Hydrogenioner (H+) spiller en kritisk rolle i syre-base-reaktioner. For eksempel kan brint frigøres fra syrer som saltsyre (HCI).
Eksempler:
* Hydrogenering af en alken: Ethen (C2H4) reagerer med brint for at danne ethan (C2H6).
* reduktion af et metaloxid: Kobberoxid (CuO) reduceres til kobber (Cu) ved at reagere det med brint.
* forbrænding af brint: 2H2 + O2 → 2H2O
* reaktion af brint med en base: Natriumhydroxid (NaOH) reagerer med brint til dannelse af natriumhydrid (NAH) og vand (H2O).
Vigtig note:
Udtrykket "kemisk reaktion med brint" er meget generelt. For at forstå reaktionen mere fuldstændigt, skal du kende detaljerne om, hvad brint reagerer med, og hvad produkterne er.
 Varme artikler
Varme artikler
-
 Mysteriet om en Picasso afsløret af videnskabsmændKredit:Museu Picasso, Barcelona. Foto:Gasull Fotografia I sommeren 1917 i Barcelona, Picasso arbejdede på fire malerier inspireret af Ballets Russes, bruge et lignende sæt materiale til dem alle,
Mysteriet om en Picasso afsløret af videnskabsmændKredit:Museu Picasso, Barcelona. Foto:Gasull Fotografia I sommeren 1917 i Barcelona, Picasso arbejdede på fire malerier inspireret af Ballets Russes, bruge et lignende sæt materiale til dem alle, -
 Økologiske polymerscintillatorer begejstrer røntgensamfundetAmorfe polymerscintillatorer, der udviser flere radioluminescensfarver, vil bidrage til røntgenbilleder i høj opløsning. Kredit:Wei et al., doi 10.1117/1.AP.4.3.035002. Røntgendetektion er af stor
Økologiske polymerscintillatorer begejstrer røntgensamfundetAmorfe polymerscintillatorer, der udviser flere radioluminescensfarver, vil bidrage til røntgenbilleder i høj opløsning. Kredit:Wei et al., doi 10.1117/1.AP.4.3.035002. Røntgendetektion er af stor -
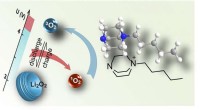 Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding
Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding -
 Forskere afslører sensor, der hurtigt opdager COVID-19-infektionNår den er knyttet til understøttende elektronik, sensoren kan trådløst overføre data til brugerens mobiltelefon via Bluetooth. Kredit:Caltech Et træk ved COVID-19-virussen, der gør den så vanskel
Forskere afslører sensor, der hurtigt opdager COVID-19-infektionNår den er knyttet til understøttende elektronik, sensoren kan trådløst overføre data til brugerens mobiltelefon via Bluetooth. Kredit:Caltech Et træk ved COVID-19-virussen, der gør den så vanskel
- Sådan konverteres ACFM til SCFM på en regnemaskine
- Nuværende generation via kvanteprotonoverførsel
- Grædende elefanter og fnisende rotter – dyr har følelser, også
- Forskere lærer at forudsige rumstrålingsniveauer
- pH-afhængig konformationsændring styrer energioverførsel i nanokrystal sensorer
- Små oplyste stregkoder identificerer molekyler ved deres blink


