Hvordan bruges loven til at måle enthly af en ønsket reaktion?
Hess's lov:
Enthalpi -ændringen af en reaktion er uafhængig af den taget vej, hvilket betyder, at det er den samme, om reaktionen forekommer i et trin eller flere trin.
hvordan det bruges til at måle entalpi:
1. Identificer kendte entalpiændringer: Find reaktioner med kendte entalpiændringer (ΔH), der kan kombineres for at danne den ønskede reaktion. Disse reaktioner findes ofte i tabeller med standard entalpi af dannelse.
2. Manipulere ligninger: Det kan være nødvendigt at:
* omvendte reaktioner: Hvis en reaktion vendes, vendes tegn på ΔH.
* Multiplicer reaktioner med en konstant: Hvis en reaktion ganges med en faktor, ganges ΔH også med denne faktor.
3. Kombiner reaktioner: Tilføj de manipulerede ligninger sammen, hvilket sikrer, at enhver fælles art på begge sider af ligningerne annullerer.
4. Beregn den samlede entalpiændring: Enthalpyændringen af den ønskede reaktion (ΔH) er summen af entalpienændringerne af de individuelle reaktioner, der blev anvendt til at danne den.
Eksempel:
Lad os sige, at vi ønsker at finde entalpiændringen til følgende reaktion:
C (s) + O2 (g) → CO2 (g) (ønsket reaktion)
Vi kender følgende reaktioner og deres entalpi ændrer sig:
1.
2. CO (g) + 1/2 o2 (g) → CO2 (g) ΔH =-283,0 kJ/mol
For at få den ønskede reaktion kan vi:
1. Forlad reaktion 2 som den er.
2. Multiplicer reaktion 1 med 2.
Nu, kombineret ligningerne giver:
2C (s) + O2 (g) → 2co (g) ΔH =-221,0 kJ/mol
2co (g) + o2 (g) → 2Co2 (g) ΔH =-566,0 kJ/mol
C (s) + O2 (g) → CO2 (g) ΔH =-787,0 kJ/mol
Derfor er entalpienændringen af den ønskede reaktion -787,0 kJ/mol.
Nøglepunkter:
* Hess's lov er et kraftfuldt værktøj til beregning af entalpiændringer, selv for reaktioner, der er vanskelige eller umulige at måle direkte.
* Det er afhængig af princippet om bevarelse af energi, hvilket betyder, at den samlede entalpiændring for en reaktion er den samme uanset den vej, der er taget.
* Forståelse af entalpi af dannelsestabeller og hvordan man manipulerer kemiske ligninger er afgørende for at bruge Hess's lov.
Sidste artikelHvad er typer petroleumsether ved kogepunkt?
Næste artikelEr den ydre kerne lavet af fast metal?
 Varme artikler
Varme artikler
-
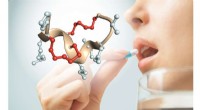 Peptider, der kan tages som en pilleStruktur af et dobbeltbro-peptid, der ikke nedbrydes af enzymer i mave og tarme. De to stabiliserende kemikaliebroer er vist med rødt. Kredit:C. Heinis (EPFL) Peptider er korte kæder af aminosyrer
Peptider, der kan tages som en pilleStruktur af et dobbeltbro-peptid, der ikke nedbrydes af enzymer i mave og tarme. De to stabiliserende kemikaliebroer er vist med rødt. Kredit:C. Heinis (EPFL) Peptider er korte kæder af aminosyrer -
 Forskere udvikler en modulær metal-organisk ramme med højeste elektronladningsmobiliteter nogensin…Til venstre, et scanning elektronmikroskopi (SEM) billede af en jern BDP MOF krystal; til højre, en jern BDP MOF enkeltkrystal enhed bundet til en platin mikroelektrode array. Kredit:Berkeley Lab
Forskere udvikler en modulær metal-organisk ramme med højeste elektronladningsmobiliteter nogensin…Til venstre, et scanning elektronmikroskopi (SEM) billede af en jern BDP MOF krystal; til højre, en jern BDP MOF enkeltkrystal enhed bundet til en platin mikroelektrode array. Kredit:Berkeley Lab -
 Machine-learning-metoden skaber en indlærelig kemisk grammatik til at bygge syntetiserbare monomere…Kredit:Pixabay/CC0 Public Domain Kemiske ingeniører og materialeforskere leder konstant efter det næste revolutionerende materiale, kemikalier og lægemidler. Fremkomsten af maskinlæringstilgange
Machine-learning-metoden skaber en indlærelig kemisk grammatik til at bygge syntetiserbare monomere…Kredit:Pixabay/CC0 Public Domain Kemiske ingeniører og materialeforskere leder konstant efter det næste revolutionerende materiale, kemikalier og lægemidler. Fremkomsten af maskinlæringstilgange -
 Detaljeret billede afslører, hvordan tandemaljen er stærk nok til at holde livet udPIC -kortlægning, som måler biominerale krystalorienteringer og tildeler forskellige farver til forskellige rotationsvinkler, afslører, at krystallerne i tandemaljen ikke er perfekt justeret. Kredit:P
Detaljeret billede afslører, hvordan tandemaljen er stærk nok til at holde livet udPIC -kortlægning, som måler biominerale krystalorienteringer og tildeler forskellige farver til forskellige rotationsvinkler, afslører, at krystallerne i tandemaljen ikke er perfekt justeret. Kredit:P
- Er syre et naturligt fremstillet fast stof, der har regelmæssigt arrangement af partikler i det?
- Automatiseret sygdomsdetektion i majs
- Australien lover at fortsætte med at udvinde kul trods klimaadvarsel
- WHO siger, at luftforurening dræber 7 millioner om året, skærper retningslinjerne
- Hvad er de gode holdninger hos en forskere?
- Sporing af et netværk på 100.000 mutanter


