Hvad er KA i kemi?
Definition:
Ka er ligevægtskonstanten til dissociation af en syre (HA) i vand:
`` `
Ha (aq) + H2O (l) ⇌ H3O + (aq) + a- (aq)
`` `
hvor:
* ha er syren
* H2O er vand
* H3O+ er hydroniumionen
* a- er den konjugate base af syren
Formel:
`` `
Ka =[H3O+] [a-] / [ha]
`` `
hvor:
* [H3O+] er koncentrationen af hydroniumioner
* [a-] er koncentrationen af den konjugatbase
* [ha] er koncentrationen af den uudskilte syre
Fortolkning:
* Større KA -værdi: Angiver en stærkere syre, hvilket betyder, at den adskiller sig lettere i opløsningen og producerer en højere koncentration af hydroniumioner.
* mindre KA -værdi: Angiver en svagere syre, hvilket betyder, at den adskiller sig mindre let, hvilket resulterer i en lavere koncentration af hydroniumioner.
Betydning:
KA er en afgørende parameter for at forstå følgende:
* syrestyrke: Højere KA indikerer en stærkere syre.
* ph af opløsninger: KA kan bruges til at beregne pH i en opløsning, der indeholder en svag syre.
* ligevægtsreaktioner: KA bruges til at bestemme omfanget af dissociation og de relative mængder reaktanter og produkter i ligevægt.
Eksempler:
* stærke syrer Ligesom saltsyre (HCI) har meget store Ka -værdier (større end 1).
* svage syrer Ligesom eddikesyre (CH3COOH) har mindre Ka-værdier (ca. 1,8 x 10^-5).
Bemærk:
PKA er den negative logaritme af Ka (PKA =-log ka). Det er en mere praktisk måde at udtrykke syrestyrke, da den bruger en mindre række af værdier.
 Varme artikler
Varme artikler
-
 Kontaktsporingssystem for kemisk eksponering i miljøetEmory-forskere kunne identificere personer, der tog forskellige medikamenter, baseret på mønsteret af lægemiddelmetabolitter efterladt i kroppen. Medicinen omfattede acetaminophen, det antidepressive
Kontaktsporingssystem for kemisk eksponering i miljøetEmory-forskere kunne identificere personer, der tog forskellige medikamenter, baseret på mønsteret af lægemiddelmetabolitter efterladt i kroppen. Medicinen omfattede acetaminophen, det antidepressive -
 Video:Du bruger desinfektionsmidler forkert. Her er hvad du faktisk skal gøreKredit:The American Chemical Society Jo da, du har et produkt, der siger dræber bakterier under din vask, men vil det virkelig ødelægge den nye coronavirus på overflader? Det viser sig, at hvis d
Video:Du bruger desinfektionsmidler forkert. Her er hvad du faktisk skal gøreKredit:The American Chemical Society Jo da, du har et produkt, der siger dræber bakterier under din vask, men vil det virkelig ødelægge den nye coronavirus på overflader? Det viser sig, at hvis d -
 Opdeling og vækst af syntetiske vesiklerKredit:Wiley En stor udfordring for produktionen af syntetiske celler er, at de skal kunne dele sig for at få afkom. I journalen Angewandte Chemie , et team fra Heidelberg har nu introduceret
Opdeling og vækst af syntetiske vesiklerKredit:Wiley En stor udfordring for produktionen af syntetiske celler er, at de skal kunne dele sig for at få afkom. I journalen Angewandte Chemie , et team fra Heidelberg har nu introduceret -
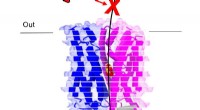 Forskere opdager, hvordan malariaparasitter importerer sukkerStruktur af transportproteinet PfHT1 i kompleks med sukker D-glucose. Kredit:David Drew Forbruget af sukker er en grundlæggende kilde til brændstof i de fleste levende organismer. I malariaparasit
Forskere opdager, hvordan malariaparasitter importerer sukkerStruktur af transportproteinet PfHT1 i kompleks med sukker D-glucose. Kredit:David Drew Forbruget af sukker er en grundlæggende kilde til brændstof i de fleste levende organismer. I malariaparasit
- Kan du sige det på tv? Højesteret debatterer
- Hvad er en egenskab ved neutron?
- Hvad er skæbnen for zink?
- Ved hjælp af lys, røde blodlegemer og et honningbipeptid til at levere terapeutiske proteiner
- Forskere opnår nye resultater på dielektronisk rekombinationspræcisionsspektroskopi
- Vådområder spiller en afgørende rolle i kulstoflagring, undersøgelse finder


