Hvilken region er der mest sandsynligt, at der kaldes en elektron?
Her er en sammenbrud:
* Elektronsky: Dette er en visuel repræsentation af sandsynligheden for at finde et elektron i en bestemt region omkring kernen. Det er ikke et solidt objekt, men snarere et uklar, tredimensionelt rum, hvor elektronet mest sandsynligt er placeret.
* orbital: Dette er et mere specifikt udtryk, der beskriver et specifikt rumområde omkring kernen, hvor en elektron har en stor sandsynlighed for at blive fundet. Hver orbital har en tydelig form og energiniveau.
Den nøjagtige form og størrelse af en elektronsky eller orbital afhænger af energiniveauet og typen af orbital (S, P, D, F).
Sidste artikelHvor mange valenselektroner har atomer i periode 1?
Næste artikelHar SR en høj elektronaffinitet eller lav affinitet?
 Varme artikler
Varme artikler
-
 Forskere tager skridt mod helt vedvarende energiL til R, Professor Max Garcia-Melchor og ph.d. Kandidat, Michael Craig, Trinity College Dublin, søger efter den grønne kugle-katalysator. Kredit:Trinity College Dublin Forskere fra Trinity College
Forskere tager skridt mod helt vedvarende energiL til R, Professor Max Garcia-Melchor og ph.d. Kandidat, Michael Craig, Trinity College Dublin, søger efter den grønne kugle-katalysator. Kredit:Trinity College Dublin Forskere fra Trinity College -
 Sådan afkøles en smartphonePrøve af materialet. Kredit:NUST MISIS NUST MISIS-forskere har udviklet kompositter, der leder varme mange gange bedre end deres modstykker og endda er genstand for enkel og billig forarbejdning.
Sådan afkøles en smartphonePrøve af materialet. Kredit:NUST MISIS NUST MISIS-forskere har udviklet kompositter, der leder varme mange gange bedre end deres modstykker og endda er genstand for enkel og billig forarbejdning. -
 Grønt materiale til køling identificeretKredit:CC0 Public Domain Forskere fra Storbritannien og Spanien har identificeret et miljøvenligt fast stof, der kan erstatte de ineffektive og forurenende gasser, der bruges i de fleste køleskabe
Grønt materiale til køling identificeretKredit:CC0 Public Domain Forskere fra Storbritannien og Spanien har identificeret et miljøvenligt fast stof, der kan erstatte de ineffektive og forurenende gasser, der bruges i de fleste køleskabe -
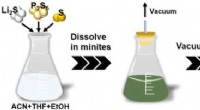 Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele
Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele
- Optøning af permafrostmikrobiomer brænder klimaændringer
- Kan rædsel gøre dig glad?
- Hvad bruger vi lysår til at måle?
- Forskere opdager nye yttrium-hydrogen-forbindelser med implikationer for højtryks-superledning
- Tættere på Jorden:En ny teknik til at undersøge zoner med ultralav hastighed ved Jordens kerne-ka…
- NASA-rumfartøj begiver sig ud på en ringskimmemission ved Saturn


