Hvad er kemisk kulsyre?
Her er en sammenbrud:
proces:
1. reaktanter: Processen involverer typisk reaktion af A carbonat eller bicarbonatsalt (f.eks. natriumbicarbonat, NAHCO3) med en syre .
2. reaktion: Reaktionen mellem carbonat/bicarbonat og syre genererer CO2 -gas , som derefter opløses i væsken.
3. Carbonation: Den opløste CO2 giver væsken sin karakteristiske fizzy, sprudlende og let sure kvaliteter.
Eksempler:
* bagepulver og eddike: Det klassiske vulkaneksperiment demonstrerer denne proces. Blanding af bagepulver (natriumbicarbonat) med eddike (eddikesyre) frigiver CO2, hvilket får blandingen til at boble og skum.
* kulsyreholdige drikkevarer: Mens de fleste kommercielt producerede sodavand er kulsyreholdige ved hjælp af CO2 -gas under tryk, bruger nogle kunsthåndværkede drikkevarer kemiske carbonationsteknikker til en unik smagsprofil.
Fordele:
* Naturlig kulsyre: Kemisk carbonation kan producere en mere naturlig-smagende kulsyre sammenlignet med den tvungne carbonationsmetode, der anvendes i mange sodavand.
* smagskontrol: Brug af forskellige carbonater og syrer giver mulighed for finjustering af smag og surhedsgrad i det endelige produkt.
Ulemper:
* Begrænset kontrol: Kemisk carbonation kan være mindre præcis end andre metoder, hvilket gør det mere udfordrende at opnå ensartede kulsyre.
* reaktionstid: Reaktionen mellem carbonat og syre kan tage tid, hvilket påvirker effektiviteten af carbonationsprocessen.
generelt:
Kemisk kulsyre er en unik og ofte overset metode til kulsyrevæsker, der tilbyder interessante muligheder for naturlige og smagfulde kulsyreholdige drikkevarer. Det er et fascinerende eksempel på kemi i handling, der skaber fizzy og forfriskende drikkevarer.
Sidste artikelReagerer elementet sølv med ilt og vand?
Næste artikelKan ozon dræbe svamp i vand?
 Varme artikler
Varme artikler
-
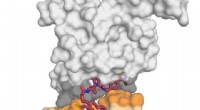 Et dødskys for at bedøve de undrugbareBilledet viser E3 -ligaseproteinet VHL (i gråt) i kompleks med det lille molekyle MZ1 (i hindbær) og kysser proteinet BRD4 (i gult). Efter at have modtaget dette dødelige kys, BRD4 er målrettet mod ne
Et dødskys for at bedøve de undrugbareBilledet viser E3 -ligaseproteinet VHL (i gråt) i kompleks med det lille molekyle MZ1 (i hindbær) og kysser proteinet BRD4 (i gult). Efter at have modtaget dette dødelige kys, BRD4 er målrettet mod ne -
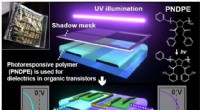 Tuning af fleksible kredsløb med lysFigur 1:Skematisk, der viser processen, der giver mulighed for præcis kontrol af de organiske transistorkarakteristika ved hjælp af lysbestråling. Indsatsen viser et fotografi af den endelige enhed. K
Tuning af fleksible kredsløb med lysFigur 1:Skematisk, der viser processen, der giver mulighed for præcis kontrol af de organiske transistorkarakteristika ved hjælp af lysbestråling. Indsatsen viser et fotografi af den endelige enhed. K -
 En elektrolytdesignstrategi til fremstilling af divalente metalbatterierBatterielektrolytter, der anvender aminbaserede chelateringsmidler, der opløser divalente kationer, viste stabil og meget reversibel plettering/stripping af Mg-metal som illustreret ved scanningselekt
En elektrolytdesignstrategi til fremstilling af divalente metalbatterierBatterielektrolytter, der anvender aminbaserede chelateringsmidler, der opløser divalente kationer, viste stabil og meget reversibel plettering/stripping af Mg-metal som illustreret ved scanningselekt -
 Nyt brændselscellekoncept bringer biologisk design til bedre elproduktionKredit:CC0 Public Domain Brændselsceller har længe været betragtet som en lovende strømkilde. Disse enheder, opfundet i 1830erne, generere elektricitet direkte fra kemikalier, såsom brint og ilt,
Nyt brændselscellekoncept bringer biologisk design til bedre elproduktionKredit:CC0 Public Domain Brændselsceller har længe været betragtet som en lovende strømkilde. Disse enheder, opfundet i 1830erne, generere elektricitet direkte fra kemikalier, såsom brint og ilt,


