Hvordan produceres et atomspektre?
1. Spændende atomerne
* Energiabsorption: Atomer i deres jordtilstand (laveste energiniveau) absorberer energi. Dette kan ske gennem forskellige metoder:
* Opvarmning: Ved at føre en elektrisk strøm gennem en gas, bruge en flamme eller udsætte prøven for høje temperaturer.
* Elektrisk udladning: Påfører en høj spænding på en gas.
* bombardement: Brug af en stråle af elektroner eller fotoner til at slå atomerne.
* Energiniveau: De absorberede energi fremmer elektroner fra deres jordtilstand til højere energiniveau (ophidsede tilstande). Disse ophidsede stater er ustabile.
2. Emission af lys
* afslapning: De ophidsede elektroner skifter hurtigt tilbage til lavere energiniveau.
* fotonemission: Når en elektron falder fra et højere energiniveau til et lavere, frigiver det den overskydende energi som en foton af lys. Fotonens energi svarer nøjagtigt til energiforskellen mellem de to niveauer.
* specifikke bølgelængder: Hvert element har et unikt sæt energiniveauer, hvilket resulterer i emission af lys ved specifikke bølgelængder. Dette er grundlaget for atomspektroskopi, der kan identificere elementer i en prøve.
3. Observerer spektret
* spektroskop: En enhed kaldet et spektroskop adskiller det udsendte lys i dets komponentbølgelængder.
* spektrale linjer: Det udsendte lys forekommer som lyse linjer (emissionsspektrum) ved specifikke bølgelængder, der repræsenterer energiovergange inden for atomet.
* Absorptionsspektrum: Hvis lys passerer gennem en prøve af atomer, absorberer atomerne lys ved specifikke bølgelængder svarende til deres energiovergange. Dette resulterer i mørke linjer (absorptionsspektrum) mod en kontinuerlig baggrund.
nøglekoncepter
* Kvantisering: Atomer kan kun eksistere i specifikke energiniveauer. Energiovergange mellem disse niveauer er diskrete, hvilket resulterer i specifikke bølgelængder af lys.
* kvantemodel: Begrebet kvantiseret energiniveau forklarer, hvorfor hvert element har et unikt atomspektrum.
applikationer
* Identificering af elementer: Atomspektre er som fingeraftryk for elementer, der giver forskere mulighed for at identificere deres tilstedeværelse og sammensætning i forskellige prøver.
* Astrofysik: Spektre af stjerner og andre himmelobjekter afslører deres kemiske sammensætning, temperatur og bevægelse.
* Analytisk kemi: Atomspektroskopi bruges til kvantitativ analyse på forskellige områder, såsom miljøovervågning, fødevarevidenskab og klinisk kemi.
Sidste artikelHvilke gasser findes ikke på Uranus?
Næste artikelHvad er definitionen af oliekant?
 Varme artikler
Varme artikler
-
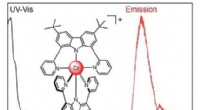 Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S
Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S -
 Ny strategi forbedrer stabiliteten af platingruppemetalkatalysatorerKredit:ACS For nylig, en gruppe ledet af Prof. kalcinering, og udviklede en ny strategi for at forbedre stabiliteten af platinagruppemetaller (PGMer) katalysatorer. Denne undersøgelse blev offe
Ny strategi forbedrer stabiliteten af platingruppemetalkatalysatorerKredit:ACS For nylig, en gruppe ledet af Prof. kalcinering, og udviklede en ny strategi for at forbedre stabiliteten af platinagruppemetaller (PGMer) katalysatorer. Denne undersøgelse blev offe -
 Forskere bruger en blender til at afsløre, hvad der er i vores smartphonesForskere brugte en blender til at male en smartphone til støv for at afsløre dens præcise indhold. Kredit:University of Plymouth Hvert år, 1,4 milliarder mobiltelefoner produceres rundt om i verde
Forskere bruger en blender til at afsløre, hvad der er i vores smartphonesForskere brugte en blender til at male en smartphone til støv for at afsløre dens præcise indhold. Kredit:University of Plymouth Hvert år, 1,4 milliarder mobiltelefoner produceres rundt om i verde -
 Kemikalieproducenter er imod nye tarifferKredit:CC0 Public Domain I juni, kemiske producenter konvergerede om Washington, D.C., at opfordre US Trade Representative Office (USTR) til at fjerne visse kemikalier fra en ny liste over toldsat
Kemikalieproducenter er imod nye tarifferKredit:CC0 Public Domain I juni, kemiske producenter konvergerede om Washington, D.C., at opfordre US Trade Representative Office (USTR) til at fjerne visse kemikalier fra en ny liste over toldsat
- Forskere tager imod tips fra Twister for at jagte uhåndgribelige stormdata
- Chokoladeindustrien driver skovrydning af Elfenbenskysten:rapport
- Konjugerede polymerer forbedrer massespektrometri og billeddannelse
- Sådan ændres 1/4 til en decimalform
- Hvordan ville tøris reagere, når der tilføjes mere?
- Intelligent genvinding og genbrug af balsatræ


