Hvad er forskellen mellem organisk molekyle og uorganisk molekyle?
organiske molekyler:
* sammensætning: Indeholder primært carbon (c) og brint (H) Atomer, ofte bundet til andre elementer som ilt (O), nitrogen (N), svovl (er) og fosfor (P).
* struktur: Har typisk en kompleks struktur med kovalente bindinger, der danner lange kæder, ringe og forgrenede strukturer.
* Oprindelse: Normalt forbundet med levende organismer eller afledt af dem.
* Eksempler: Carbohydrater, proteiner, lipider, nukleinsyrer (DNA og RNA), methan (CH4), ethanol (C2H5OH)
uorganiske molekyler:
* sammensætning: Mangler typisk kulstof- og brintatomer, eller har dem i meget små mængder. De består ofte af metaller, ikke -metaller eller metalloider.
* struktur: Generelt har enkle strukturer med ioniske eller metalliske bindinger.
* Oprindelse: Fundet i ikke-levende verden (f.eks. klipper, mineraler, vand)
* Eksempler: Vand (H2O), salt (NaCl), kuldioxid (CO2), jernoxid (Fe2O3)
Her er en tabel, der opsummerer de vigtigste forskelle:
| Funktion | Organiske molekyler | Uorganiske molekyler |
| ---------------- | ---------------------------------------------------------------------- |
| sammensætning | Primært C og H, ofte O, N, S, P | Mangler typisk C og H, eller har dem i små mængder |
| struktur | Komplekse, kovalente bindinger, lange kæder, ringe | Enkel, ioniske eller metalliske bindinger |
| Oprindelse | Forbundet med levende organismer | Fundet i den ikke-levende verden |
Vigtig note: Der er nogle undtagelser og overlapninger. For eksempel indeholder kuldioxid (CO2) kulstof, men betragtes som uorganisk på grund af dets enkle struktur og mangel på tilknytning til livet. Nogle organiske molekyler, som urinstof, produceres af levende organismer, men har en enklere struktur.
I sidste ende er sondringen mellem organiske og uorganiske molekyler et nyttigt klassificeringssystem til at forstå den enorme mangfoldighed af kemiske forbindelser.
 Varme artikler
Varme artikler
-
 Krympefilm får grebKredit:American Chemical Society Mange mennesker husker med glæde at lege med legetøj kendt som Shrinky Dinks - plader af polystyrenplast med former, som børn kan farve, skær ud og varm i en ovn,
Krympefilm får grebKredit:American Chemical Society Mange mennesker husker med glæde at lege med legetøj kendt som Shrinky Dinks - plader af polystyrenplast med former, som børn kan farve, skær ud og varm i en ovn, -
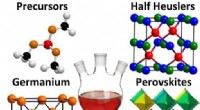 Udvikling af lavdimensionelle nanomaterialer kan revolutionere fremtidige teknologierNogle af de uorganiske halvledere under undersøgelse af Vela og kolleger. Kredit:Ames Laboratory Javier Vela, forsker ved U.S. Department of Energys Ames Laboratory, mener forbedringer i computerp
Udvikling af lavdimensionelle nanomaterialer kan revolutionere fremtidige teknologierNogle af de uorganiske halvledere under undersøgelse af Vela og kolleger. Kredit:Ames Laboratory Javier Vela, forsker ved U.S. Department of Energys Ames Laboratory, mener forbedringer i computerp -
 Forskning giver håb om enklere kræftdiagnose og behandlingRyan Kelly i sit laboratorium. Kredit:Jaren Wilkey/BYU Overvågning af kræft kan ofte være en påtrængende og udmattende proces for patienter. Men med Brigham Young University kemiprofessor Ryan Kel
Forskning giver håb om enklere kræftdiagnose og behandlingRyan Kelly i sit laboratorium. Kredit:Jaren Wilkey/BYU Overvågning af kræft kan ofte være en påtrængende og udmattende proces for patienter. Men med Brigham Young University kemiprofessor Ryan Kel -
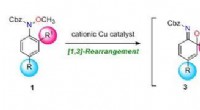 Effektiv syntese af multisubstituerede aniliner ved domino-omlejringMultisubstituerede aniliner (ortho-anisidiner). Kredit:Tohoku University Aniliner er blevet meget brugt i medicin, især i acetaminophen smertestillende midler. De bruges også i organiske materiale
Effektiv syntese af multisubstituerede aniliner ved domino-omlejringMultisubstituerede aniliner (ortho-anisidiner). Kredit:Tohoku University Aniliner er blevet meget brugt i medicin, især i acetaminophen smertestillende midler. De bruges også i organiske materiale
- Er Elon Musk og SpaceX ved at ødelægge vores syn på nattehimlen?
- Hvad er densiteten af fyrretræ?
- Hvorfor skabes metamorfe klipper dybt i skorpe ikke på overfladen?
- Livet i disse stjernesystemer kunne have set Jorden
- Kulgaslagringshule er den bedste måde at opnå ren energi fra et fossilt brændstof
- Når det kommer til hvordan pizza ser ud, betyder ost


