Hvor mange mol mangan er indeholdt i 0 punkt 1 hydreret II -sulfat MnsO4 4H2O, der har en RFM 223?
1. Bestem den molære masse af mangan (MN):
* Den molære masse af Mn er ca. 54,94 g/mol.
2. Beregn molen af mangan i 0,1 g af det hydratiserede salt:
* Trin 1:Find masseprocenten af MN i det hydratiserede salt:
* Molær masse af Mnso₄ · 4H₂O =223 g/mol (givet)
* Masseprocent af Mn =(molmasse Mn / molær masse af mnso₄ · 4H₂o) * 100%
* Masseprocent af Mn =(54,94 g/mol/223 g/mol) * 100% ≈ 24,6%
* Trin 2:Beregn massen af Mn i 0,1 g af det hydratiserede salt:
* Masse Mn =0,1 g * 24,6% =0,0246 g
* Trin 3:Beregn molen på MN:
* Mol mn =masse af mn / molær masse af Mn
* Mol mn =0,0246 g/54,94 g/mol ≈ 0,000448 mol
Derfor er ca. 0,000448 mol mangan indeholdt i 0,1 g mnso₄ · 4H₂o.
 Varme artikler
Varme artikler
-
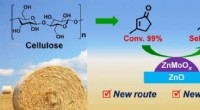 Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake
Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake -
 Forskere finder lovende nanopartikelkandidater til kuldioxidopsamling og omdannelseOriginalt kunstværk fra University of Pittsburgh, der viser en kobberbaseret bimetallisk nanopartikel designet til at adsorbere og aktivere kuldioxid, dukkede op på forsiden af ChemSusChem i april 2
Forskere finder lovende nanopartikelkandidater til kuldioxidopsamling og omdannelseOriginalt kunstværk fra University of Pittsburgh, der viser en kobberbaseret bimetallisk nanopartikel designet til at adsorbere og aktivere kuldioxid, dukkede op på forsiden af ChemSusChem i april 2 -
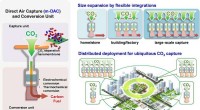 Membraner til at opfange kuldioxid fra luftenTeknologiske løsninger for CO2-emissionen til atmosfæren bør omfatte forskellige tilgange, da der ikke findes én silver bullet-løsning. I dette arbejde, forskere fra I2CNER, Kyushu University og NanoM
Membraner til at opfange kuldioxid fra luftenTeknologiske løsninger for CO2-emissionen til atmosfæren bør omfatte forskellige tilgange, da der ikke findes én silver bullet-løsning. I dette arbejde, forskere fra I2CNER, Kyushu University og NanoM -
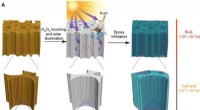 En ny måde at gøre træ gennemsigtigt på, stærkere og lettere end glasSkematisk illustration af fremstilling af gennemsigtigt træ og demonstration af dets mønstre. (A) Skematisk illustration af denne enkle, men effektive, miljøvenlig, skalerbar, og billig metode til fre
En ny måde at gøre træ gennemsigtigt på, stærkere og lettere end glasSkematisk illustration af fremstilling af gennemsigtigt træ og demonstration af dets mønstre. (A) Skematisk illustration af denne enkle, men effektive, miljøvenlig, skalerbar, og billig metode til fre
- Når to oceaniske plader afviger?
- Hvordan administrerende direktørs politiske holdninger påvirker deres internationale aftaler
- Hvilken stat har de største jernmalmsforekomster?
- Hvordan adskiller diffusion af gasser sig i dag og natplanter?
- Molekylær og isotopisk tegn på mælk, kød og planter i forhistoriske fødevaresystemer
- Irans sekulære skift:Ny undersøgelse afslører enorme ændringer i religiøs overbevisning


