Hvorfor salt er spredt på frosset overflade?
Sådan fungerer det:
1. salt opløses i vand: Når salt (natriumchlorid) drysses på is, opløses det i det tynde vandlag, der naturligt dannes på isens overflade.
2. ioner forstyrrer vandmolekyler: Det opløste salt bryder ned i ioner (natrium og chlorid). Disse ioner forstyrrer dannelsen af den regelmæssige, krystallinske struktur, som is skal forblive frosset.
3. Nedre frysepunkt: Denne forstyrrelse gør det sværere for vandmolekyler at fryse, hvilket effektivt sænker vandets frysepunkt.
4. smeltning af isen: Når frysepunktet sænkes, begynder isen at smelte, selvom temperaturen er under 32 ° F (0 ° C).
Kort sagt, salt får isen til at smelte ved at sænke det frysepunkt for vand. Denne proces hjælper med at gøre veje og fortove mere sikre ved at fjerne isen og skabe en mindre glat overflade.
 Varme artikler
Varme artikler
-
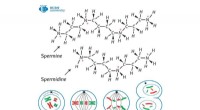 Biokemiker opdager et lovende enzym til at bekæmpe kræftcellerKredit:RUDN Universitet En biokemiker fra RUDN Universitet har undersøgt kemiske stoffers stimulerende virkning på det kataboliske enzym PAO (polyaminoxidase). Resultaterne kan bidrage til udvikli
Biokemiker opdager et lovende enzym til at bekæmpe kræftcellerKredit:RUDN Universitet En biokemiker fra RUDN Universitet har undersøgt kemiske stoffers stimulerende virkning på det kataboliske enzym PAO (polyaminoxidase). Resultaterne kan bidrage til udvikli -
 De fleste proteinoplysninger, der nogensinde er fanget fra en enkelt celle takket være ny nanoPOTS-…Chippen, der indeholder flere brønde, hvor proteiner fra enkelte celler adskilles til yderligere analyse. Kredit:PNNL Forskere har fået en række nøgleoplysninger om proteiner, alle cellers molekyl
De fleste proteinoplysninger, der nogensinde er fanget fra en enkelt celle takket være ny nanoPOTS-…Chippen, der indeholder flere brønde, hvor proteiner fra enkelte celler adskilles til yderligere analyse. Kredit:PNNL Forskere har fået en række nøgleoplysninger om proteiner, alle cellers molekyl -
 Forskere syntetiserer et materiale, der er i stand til at nedbryde nervestoffer i vandKredit:CC0 Public Domain Et team fra Institute of Molecular Science (ICMol) fra University of Valencia er lykkedes med at syntetisere et nyt porøst materiale, der muliggør og styrer nedbrydning af
Forskere syntetiserer et materiale, der er i stand til at nedbryde nervestoffer i vandKredit:CC0 Public Domain Et team fra Institute of Molecular Science (ICMol) fra University of Valencia er lykkedes med at syntetisere et nyt porøst materiale, der muliggør og styrer nedbrydning af -
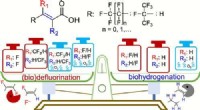 Under anaerobe forhold kan almindelige mikrobielle samfund bryde den ultra-stærke kulstof-fluor-bin…Kredit:Yaochun Yu et al., Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c05509 Ingeniører ved University of California Riverside er de første til at rapportere selektiv nedbrydning
Under anaerobe forhold kan almindelige mikrobielle samfund bryde den ultra-stærke kulstof-fluor-bin…Kredit:Yaochun Yu et al., Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c05509 Ingeniører ved University of California Riverside er de første til at rapportere selektiv nedbrydning
- Hvorfor kan vi ikke generere al vores energi fra vindkraft?
- Hvad sker der, når nikkel opvarmes?
- Hvilket er ikke et resultat af miljøet, der ændrer en fænotype?
- Antag, at du træder en 25 kg cykel på 1,5 m. Finder cyklens kinetiske energi?
- Liste over tre andre stoffer, der end sedimenter, hvor organismer kan bevares?
- Hvad sker der med massen af et grundstof, når det brænder?


