Hvorfor er halogenerne så reaktive og ædle gasser ikke reaktive?
halogener:
* Elektronkonfiguration: Halogener (gruppe 17) har syv valenselektroner (elektroner i deres yderste skal). De er kun en elektron væk fra at opnå en stabil, fuld ydre skal, som de ædle gasser.
* tendens til at få elektroner: For at opnå stabilitet har halogener en stærk tendens til at vinde en elektron, der danner en negativ ion (en anion). Dette gør dem meget reaktive, da de let reagerer med andre elementer for at afslutte deres ydre skal.
* Høj elektronegativitet: Halogener har høj elektronegativitet, hvilket betyder, at de har en stærk tiltrækning for elektroner. Dette bidrager til deres evne til at trække elektroner væk fra andre atomer, danne bindinger og deltage i reaktioner.
ædle gasser:
* Elektronkonfiguration: Ædle gasser (gruppe 18) har en komplet ydre skal af elektroner. Dette gør dem usædvanligt stabile, da deres elektronkonfiguration allerede er afbalanceret og lav i energi.
* Ingen tendens til at vinde eller miste elektroner: Da de har en fuld ydre skal, har de ikke behov for at vinde eller miste elektroner for at blive mere stabile. Dette gør dem ekstremt ureaktive.
Kortfattet:
Halogener er reaktive, fordi de er ivrige efter at få en elektron for at opnå en stabil elektronkonfiguration. Noble gasser er ureaktive, fordi de allerede har en stabil elektronkonfiguration og ikke behøver at vinde eller miste elektroner.
Sidste artikelHvad er en reaktiv ikke -metal?
Næste artikelHvorfor er aspirin mere reaktiv end benzen?
 Varme artikler
Varme artikler
-
 Et nyt materiale til at printe mekanisk robuste og formskiftende strukturerKredit:Zhang et al. I de seneste år, 3-D print har åbnet interessante nye muligheder for storskala produktion af elektroniske komponenter, samt af en række andre genstande. Til denne ende, forsker
Et nyt materiale til at printe mekanisk robuste og formskiftende strukturerKredit:Zhang et al. I de seneste år, 3-D print har åbnet interessante nye muligheder for storskala produktion af elektroniske komponenter, samt af en række andre genstande. Til denne ende, forsker -
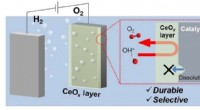 Afskærmning af iltproduktion for at holde brint på vejDen porøse belægning øger holdbarheden af oxygendannende katalysatorer, som industrien ivrigt efterspørger. Kredit:KAUST En porøs ceriumbaseret belægning øger holdbarheden af oxygendannende ka
Afskærmning af iltproduktion for at holde brint på vejDen porøse belægning øger holdbarheden af oxygendannende katalysatorer, som industrien ivrigt efterspørger. Kredit:KAUST En porøs ceriumbaseret belægning øger holdbarheden af oxygendannende ka -
 Forskere udvikler en ny clip-on-enhed til smartphones til analyse af sædcellerKredit:Lukasz Pawel Szczepanski, Shutterstock Mandlig infertilitetstest udføres i øjeblikket udelukkende i laboratorier, kræver flere besøg og flere dage for at få et resultat. Det EU-finansierede
Forskere udvikler en ny clip-on-enhed til smartphones til analyse af sædcellerKredit:Lukasz Pawel Szczepanski, Shutterstock Mandlig infertilitetstest udføres i øjeblikket udelukkende i laboratorier, kræver flere besøg og flere dage for at få et resultat. Det EU-finansierede -
 Voks på, smelte afForskere fra Drexel University, Purdue University og Oregon State University har opdaget, at tilsætning af paraffinolie til blandingen til vejbeton kan give den evnen til at smelte is og sne, når temp
Voks på, smelte afForskere fra Drexel University, Purdue University og Oregon State University har opdaget, at tilsætning af paraffinolie til blandingen til vejbeton kan give den evnen til at smelte is og sne, når temp


