Hvorfor er aspirin mere reaktiv end benzen?
* benzens aromatiske stabilitet: Benzen har en meget stabil struktur på grund af dens delokaliserede PI -elektroner, hvilket skaber en resonanshybrid. Denne delokalisering gør det mindre tilbøjeligt til elektrofilt angreb, som er den typiske måde, aromatiske forbindelser reagerer på.
* aspirins funktionelle grupper: Aspirin har flere funktionelle grupper, der gør det mere reaktivt end benzen. Disse inkluderer:
* carboxylsyregruppe: Carboxylsyre-gruppen (-COOH) er sur og tilbøjelig til reaktioner som esterificering, amidering og saltdannelse.
* Estergruppe: Estergruppen (-coo-) kan gennemgå hydrolyse og andre reaktioner.
* Elektrofilt angreb: Mens benzen kan gennemgå elektrofil aromatisk substitution, kræver det barske tilstande og stærke elektrofiler. Aspirin med sine funktionelle grupper er mere modtagelig for elektrofilt angreb under mildere forhold.
Kortfattet: Benzens aromatiske stabilitet gør det mindre reaktivt, mens Aspirins funktionelle grupper øger dens reaktivitet. Derfor er aspirin mere reaktiv end benzen.
 Varme artikler
Varme artikler
-
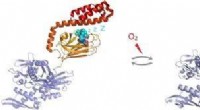 S-glutathionylering af human-inducerbar Hsp70 afslører reguleringsmekanisme, der involverer C-termi…Figur:Under oxidative stressforhold, den molekylære chaperon Hsp70 undergår post-translationel modifikation af cysteinrester ved tilsætning af tripeptidet glutathion. Glutathionylering inden for det s
S-glutathionylering af human-inducerbar Hsp70 afslører reguleringsmekanisme, der involverer C-termi…Figur:Under oxidative stressforhold, den molekylære chaperon Hsp70 undergår post-translationel modifikation af cysteinrester ved tilsætning af tripeptidet glutathion. Glutathionylering inden for det s -
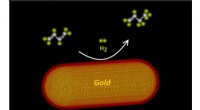 Tværfagligt samarbejde fører til katalysatorer, der er op til 50 gange mere effektiveKemiske reaktioner forekommer på overfladen af bimetalliske nanopartikler. Forskere fandt ud af, at arrangering af de to metaller i et kerneskalledesign gør disse katalysatorer op til 50 gange mere
Tværfagligt samarbejde fører til katalysatorer, der er op til 50 gange mere effektiveKemiske reaktioner forekommer på overfladen af bimetalliske nanopartikler. Forskere fandt ud af, at arrangering af de to metaller i et kerneskalledesign gør disse katalysatorer op til 50 gange mere -
 Teknologi til fremstilling af aluminiummatrixkompositter af nye råvarerAlexander Gromov, projektleder, professor ved NUST MISIS. Kredit:Sergey Gnuskov/NUST MISIS Materialeforskere fra NUST MISIS har præsenteret en ny teknologi til fremstilling af aluminiummatrixkompo
Teknologi til fremstilling af aluminiummatrixkompositter af nye råvarerAlexander Gromov, projektleder, professor ved NUST MISIS. Kredit:Sergey Gnuskov/NUST MISIS Materialeforskere fra NUST MISIS har præsenteret en ny teknologi til fremstilling af aluminiummatrixkompo -
 Potentialet ved fleksible OLED'er som et innovativt overfladematerialeKredit:Vashchig, Shutterstock Beklædning med høj synlighed er et vigtigt element i enhver motorcyklists sikkerhedsrutine. Sådanne produkter indeholder normalt reflekterende strimler for øget synli
Potentialet ved fleksible OLED'er som et innovativt overfladematerialeKredit:Vashchig, Shutterstock Beklædning med høj synlighed er et vigtigt element i enhver motorcyklists sikkerhedsrutine. Sådanne produkter indeholder normalt reflekterende strimler for øget synli
- Fysikeres algoritme forudsiger molekylers optiske egenskaber
- Hvilken type videnskabsmand er Carolus Linnaeus?
- Hvad er forholdet mellem månens overfladetyngdekraft mangel på atmosfære og temperaturområde?
- Luskede hanner adopterer kvindelignende hjerner for at narre store dyr
- Hvordan medierer grundstammer salinitetstolerance under saltstress?
- Mantle neon oplyser Jordens formation


