Har fraværet af katalysator og virkning på resultatet termisk nedbrydning kaliumchlorid?
Her er hvorfor:
* stærk ionisk binding: KCL er en ionisk forbindelse, der holdes sammen af stærke elektrostatiske attraktioner mellem kaliumkationer (K+) og chloridanioner (Cl-). Disse obligationer kræver en betydelig mængde energi for at bryde.
* Høj nedbrydningstemperatur: Nedbrydningen af KCL kræver ekstremt høje temperaturer, langt ud over, hvad der typisk er stødt på i laboratorieindstillinger.
* Ingen iboende tendens til at nedbrydes: KCL er en stabil forbindelse og nedbrydes ikke let i dens bestanddele under normale forhold.
Sammenfattende er termisk nedbrydning af kaliumchlorid ikke en mulig proces under normale omstændigheder, uanset tilstedeværelsen eller fraværet af en katalysator.
Sidste artikelHvad erstatter opvarmet luft ved ækvator?
Næste artikelHvordan ved du, at brandbarhed er en kemisk ændring?
 Varme artikler
Varme artikler
-
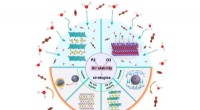 Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af
Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af -
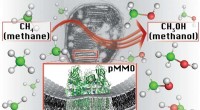 Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University
Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University -
 Vanilje får mælkedrikke til at virke sødereKredit:CC0 Public Domain Tilsætning af vanilje til sødet mælk får forbrugerne til at tro, at drikkevaren er sødere, gør det muligt at reducere mængden af tilsat sukker, ifølge forskere fra Penn
Vanilje får mælkedrikke til at virke sødereKredit:CC0 Public Domain Tilsætning af vanilje til sødet mælk får forbrugerne til at tro, at drikkevaren er sødere, gør det muligt at reducere mængden af tilsat sukker, ifølge forskere fra Penn -
 Ikke for våd, ikke for tør – plasmabehandlet brændselscelle får det helt rigtigtStudieforfatter Benjamin Zahiri, en materialeforsker Kredit:Benjamin Zahiri Brændselsceller lover som en ren, vedvarende energikilde. Men at holde dem tørre har længe været en udfordring, da de pr
Ikke for våd, ikke for tør – plasmabehandlet brændselscelle får det helt rigtigtStudieforfatter Benjamin Zahiri, en materialeforsker Kredit:Benjamin Zahiri Brændselsceller lover som en ren, vedvarende energikilde. Men at holde dem tørre har længe været en udfordring, da de pr
- Forskelle fundet i antioxidantaktiviteter af astaxanthinisomerer mod singlet oxygen
- Ingeniører fremmer indsigt i sort fosfor som et materiale til fremtidig fleksibel elektronik med ul…
- Hvad er massen af AlCl3, der dannes, når 25,0 gram Al2O3 reagerer med HCl ifølge 6HCl til 2ALCl3…
- Hvad hæver jordens temperatur?
- Sådan bestemmer du hvor mange hybrid orbitaler
- Hvad er brugen af enfasningsvariak i kredsløb?


