Hvorfor er SiO2 mere opløselig i havvand vs frisk vand?
* saltholdighed: Havvand indeholder en høj koncentration af opløste salte, primært natriumchlorid (NaCI). Disse salte øger opløsningens ionstyrke, hvilket gør den vanskeligere for SiO2 at opløses.
* ioniske interaktioner: De opløste ioner i havvand konkurrerer med SiO2 om hydrering (processen med vandmolekyler omgivende og stabiliserende ioner/molekyler). Denne konkurrence reducerer den effektive koncentration af vand, der er tilgængelig til opløsning af SiO2.
* Kompleksation: Nogle af de opløste ioner i havvand, som calcium (Ca²⁺), kan danne komplekser med opløst silica, hvilket effektivt fjerner det fra opløsning.
Kortfattet: Den høje saltholdighed og ioniske styrke af havvand gør det til et mindre gunstigt miljø til opløsning af SiO2 sammenlignet med ferskvand.
Bemærk: Mens SiO2 er mindre opløselig i havvand end i ferskvand, betragtes begge stadig relativt lavt i opløselighed. Langt de fleste silica i havet findes i form af faste partikler (f.eks. Diatomer).
Sidste artikelEr et elektron kun et navn på både neutroner og protoner?
Næste artikelKemisk formel for magnesium 2 periodat?
 Varme artikler
Varme artikler
-
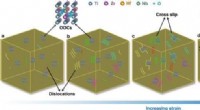 Forbedret styrke og duktilitet i en legering med høj entropi via bestilte iltkomplekserSkematisk diagram, der illustrerer mekanismen for plastisk deformation i den kubiske struktur af den iltrige high-entropy legering (HEA). a) I de ilt-høje entropylegeringer, de bestilte iltkomplekser
Forbedret styrke og duktilitet i en legering med høj entropi via bestilte iltkomplekserSkematisk diagram, der illustrerer mekanismen for plastisk deformation i den kubiske struktur af den iltrige high-entropy legering (HEA). a) I de ilt-høje entropylegeringer, de bestilte iltkomplekser -
 Opfindelse udløst af COVID-19-pandemi desinficerer overflader sikkert kontinuerligtKredit:Pixabay/CC0 Public Domain En opfindelse til at påføre plasma på genstande, der ofte berøres, til kontinuerlig desinfektion kunne give en sikker og effektiv, ikke-kemisk måde at reducere pat
Opfindelse udløst af COVID-19-pandemi desinficerer overflader sikkert kontinuerligtKredit:Pixabay/CC0 Public Domain En opfindelse til at påføre plasma på genstande, der ofte berøres, til kontinuerlig desinfektion kunne give en sikker og effektiv, ikke-kemisk måde at reducere pat -
 Issikker belægning til store strukturer er afhængig af en smuk demonstration af mekanikAnish Tuteja, lektor i materialevidenskab og teknik ved University of Michigan, og hans forskergruppe har lavet en belægning, der kaster is fra store overflader. Kredit:Joseph Xu/Michigan Engineering,
Issikker belægning til store strukturer er afhængig af en smuk demonstration af mekanikAnish Tuteja, lektor i materialevidenskab og teknik ved University of Michigan, og hans forskergruppe har lavet en belægning, der kaster is fra store overflader. Kredit:Joseph Xu/Michigan Engineering, -
 Diagnostisk værktøj til coronavirus gør et vigtigt skridt fremadKredit:CC0 Public Domain Forskere ved University of Warwick har demonstreret, at et potentielt diagnostisk værktøj til at opdage COVID-19 ved hjælp af sukker vil fungere med en virus frem for kun
Diagnostisk værktøj til coronavirus gør et vigtigt skridt fremadKredit:CC0 Public Domain Forskere ved University of Warwick har demonstreret, at et potentielt diagnostisk værktøj til at opdage COVID-19 ved hjælp af sukker vil fungere med en virus frem for kun
- Eksperter opfordrer til en revision af pesticidreglerne
- Gennemgang identificerer huller i vores forståelse af, hvordan maskinlæring kan hjælpe med aktiev…
- Uanset hvilke nye funktioner Apple annoncerer i næste uge, disse tre er dem, der virkelig betyder n…
- I Brasilien, Amazon-brande truer tusindårige klippemalerier
- Huygens:Grundlæggende sandhed fra en fremmed måne - 2005 historisk afstamning til Titan revideret
- Simulering:Støv kunne have spredt sig jævnt over jorden efter Chicxulub -asteroiden


