Øger en katalysator altid reaktionshastigheden, eller kan den også falde?
Her er hvorfor:
* sænkning af aktiveringsenergi: Katalysatorer fungerer ved at tilvejebringe en alternativ reaktionsvej med en lavere aktiveringsenergi. Dette betyder, at flere molekyler har nok energi til at overvinde energibarrieren og reagere, hvilket fører til en hurtigere reaktionshastighed.
* ikke konsumeret: Katalysatorer forbruges ikke i reaktionen. De deltager i reaktionsmekanismen, men dukker uændrede ud i slutningen, klar til at katalysere flere reaktioner.
Vigtig note: Mens en katalysator altid øger en reaktionshastighed, gør den ikke Skift reaktionens ligevægtsposition. Det hjælper simpelthen reaktionen med at nå ligevægt hurtigere.
Lad mig vide, om du vil have flere detaljer om, hvordan katalysatorer fungerer!
Sidste artikelHvorfor er filtrat ren?
Næste artikelHvilket forventes at have de største spredningskræfter CO2 C8H18 N2 C2H6?
 Varme artikler
Varme artikler
-
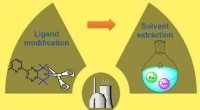 Molekyleændring kan forbedre oparbejdning af brugt nukleart brændstofKredit:Northumbria University Oparbejdningen af brugt nukleart brændstof kan blive mere sikker og mere effektiv i fremtiden, efter at forskere fandt en måde at ændre strukturen af molekyler ti
Molekyleændring kan forbedre oparbejdning af brugt nukleart brændstofKredit:Northumbria University Oparbejdningen af brugt nukleart brændstof kan blive mere sikker og mere effektiv i fremtiden, efter at forskere fandt en måde at ændre strukturen af molekyler ti -
 Smagsligheden mellem fødevarer kan sammenlignes ved hjælp af elektroencefalografiKredit:Pixabay/CC0 Public Domain Marina Domracheva og Sofya Kulikova, forskere fra HSE Universitets campus i Perm, har opdaget en ny tilgang til at analysere den opfattede lighed mellem fødevarer,
Smagsligheden mellem fødevarer kan sammenlignes ved hjælp af elektroencefalografiKredit:Pixabay/CC0 Public Domain Marina Domracheva og Sofya Kulikova, forskere fra HSE Universitets campus i Perm, har opdaget en ny tilgang til at analysere den opfattede lighed mellem fødevarer, -
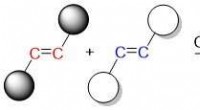 Jernkatalysator kunne gøre vigtige kemiske reaktioner billigere og mere miljøvenligeOlefinmetatesereaktionen producerer nye carbon-carbon dobbeltbindinger ved at bryde de oprindelige dobbeltbindinger og regenerere nye. Kredit:OIST En katalysator er en nøgleingrediens i mange kemis
Jernkatalysator kunne gøre vigtige kemiske reaktioner billigere og mere miljøvenligeOlefinmetatesereaktionen producerer nye carbon-carbon dobbeltbindinger ved at bryde de oprindelige dobbeltbindinger og regenerere nye. Kredit:OIST En katalysator er en nøgleingrediens i mange kemis -
 Frigivelse af lægemidler fra et supramolekylært burForskere lykkes med at konstruere et supramolekylært bur og læsse det med farmaceutisk aktiv last. I vandig opløsning, ultralydsbølger åbner buret og frigiver lægemidlet. Kredit:HHU/Robin Küng Hvo
Frigivelse af lægemidler fra et supramolekylært burForskere lykkes med at konstruere et supramolekylært bur og læsse det med farmaceutisk aktiv last. I vandig opløsning, ultralydsbølger åbner buret og frigiver lægemidlet. Kredit:HHU/Robin Küng Hvo
- Supernova SN 2018byg udløst af en helium-skal dobbelt detonation, undersøgelse finder
- Oakland, Californien, barer by fra at bruge ansigtsgenkendelse teknologi
- Hvorfor er muskelceller normalt afhængige af aerob respiration frem for fermentering?
- Ny rapport om nanomaterialer og grafen til 3D -print og additiv fremstilling
- Hvorfor går flere politikere ikke på pension? Ekspert forklarer, hvordan USA kan drage fordel af e…
- Hvilken ladning bærer hver subatomare partikel?


